A. Trắc nghiệm: (Thời gian: 15 phút)3 điểm.
Em hãy khoanh tròn vào câu trả lời đúng trong những câu sau :
Câu 1: Nhúng quỳ tím vào dung dịch natrihidroxit (NaOH) quỳ chuyển màu:
A. Đỏ B. Xanh C. Trắng . D. Vàng
Câu 2 : Để phân biệt 2 dung dịch natri sunfat và Natri cacbonat người ta có thể dùng dung dịch thuốc thử nào sau đây :
A. BaCl2 B. HCl C. NaOH D. NaCl
Câu 3 : Đơn chất nào sau đây tác dụng với dung dịch a xít sunfuric loãng sinh ra chất khí :
A. Cacbon B. Sắt C. Bạc D. Lưu huỳnh
Câu 4 : Có 4 cách sắp xếp các kim loại sau đây theo mức độ hoạt động hóa học tăng dần. Hãy chọn cách sắp xếp đúng.
A. Na, Al, Zn, Pb, Fe, Ag, Cu. B. Al, Zn, Fe, Na, Cu, Ag, Pb.
C. Ag, Cu, Pb, Zn, Fe, Al, Na. D. Ag, Cu, Pb, Fe, Zn, Al, Na.
Câu 5 : Kim loại nào hoạt động hóa học mạnh nhất trong các kim loại sau :
A. Đồng B. Magie C. Natri D. Sắt
Câu 6: Phân hủy Al(OH)3 thu được:
A. Al và O2 B. Al và H2O C. Al2 O3 và H2O D. Al2 O3 và H2
Câu 7. Hãy ghép các chữ cái A,B,C… chỉ nội dung thí nghiệm với một chữ số 1,2,3….chỉ hiện tượng xảy ra cho phù hợp.
| Nội dung thí nghiệm |
Hiện tượng xảy ra |
Kết quả |
| A. Cho dây đồng vào dd HCl |
1. Kim loại tan dần màu đỏ của kim loại mất dần,màu trắng xuất hiện. |
1……. |
| B. Cho dd Na2CO3 vào dd H2SO4 loãng |
2. dd có chất khí thoát ra. |
2……. |
| C. Cho dây nhôm vào cốc đựng dd KOH loãng |
3. Có chất kết tủa trắng xuất hiện. |
3……. |
| D. Cho dây đồng vào dd AgNO3 |
4. Kim loại tan dần và có khí bay ra |
4……. |
| E. Cho đinh sắt vào dd H2SO4 đặc nóng |
5. Không có hiện tượng gì. |
5……. |
| F. Nhỏ dd BaCl2 vào dd CuSO4 |
6. Kim loại tan dần và có khí mùi hắc bay ra |
6……. |
II. TỰ LUẬN: (
Thời gian: 30 phút) (
7 điểm)
Câu 1: 3đ. Hoàn thành các sơ đồ phản ứng theo sơ đồ sau:
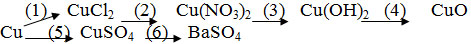 Câu 2: 2,5đ.
Câu 2: 2,5đ.
Hoà tan 4,4 gam hỗn hợp gồm Mg và MgO bằng dd HCl 7,3% vừa đủ.Sau phản ứng thu được 2,24 lít khí (ở đktc)
a) Viết các phương trình phản ứng xảy ra.
b) Tính khối lượng mỗi chất có trong hỗn hợp ban đầu.
c) Tính khối lượng dd HCl 7,3% cần dùng để trung hoà hết hỗn hợp trên.
Câu 3: 1,5đ
Để xác định thành phần phần trăm khối lượng của hỗn hợp A gồm bột Nhôm và bột Magiê, người thực hiện hai thí nghiệm sau :
- Thí nghiệm 1: cho m gam hỗn hợp A tác dụng với dung dịch H
2SO
4 loãng dư, người ta thu được1568 ml khí (đktc).
- Thí nghiệm 2: cho m gam hỗn hợp A tác dụng với dung dịch NaOH dư, sau phản ứngthấy có 0,6 g chất rắn.
Hãy xác định thành phần phần trăm khối lượng của hỗn hợp A ?
--------------------------------
ĐÁP ÁN
I. Trắc nghiệm: 3đ. (Mỗi câu trả lời đúng 0.25 điểm)
| Câu |
1 |
2 |
3 |
4 |
5 |
6 |
| Đáp án |
B |
A |
B |
D |
C |
C |
Câu7. A-5 ; B-2; C-4; D-1; E-6; F-3
II.Tự luận: 7đ
| CÂU |
ĐÁP ÁN |
ĐIỂM |
Câu 1
3đ
|
(1) Cu+Cl2 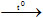 CuCl2 ; CuCl2 ;
(2)CuCl2 + 2AgNO3 → Cu(NO3)2 + 2AgCl
(3)Cu(NO3)2 + 2NaOH → Cu(OH)2 + 2NaNO3
(4)Cu(OH)2 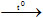 CuO +H2O CuO +H2O
(5) Cu + 2H2SO4đ/nóng → CuSO4 + SO2 + 2H2O
(6) CuSO4 + BaCl2 → BaSO4 + CuCl2 |
0,5
0,5
0,5
0,5
0,5
0,5
|
Câu 2
2,5đ
|
a)Mg + 2HCl → MgCl2 + H2 (1)
1mol : 2mol : 1mol : 1mol
MgO + 2HCl → MgCl2 + H2O (2)
1mol : 2mol : 1mol : 1mol
b) nH2= =0,1mol =0,1mol
Theo (1) nH2 = nMg = 0,1mol -> mMg = 0.1 x 24 = 2.4 g
-> mMgo = 4,4 – 2.4 = 2g
→ nMgO=2/40 = 0,05mol
c) Theo (1)nHCl= 2. 0,1=0,2mol
Theo (2)nHCl=2. 0,05 = 0,1mol
Khối lượng của axit ở cả 2 phản ứng là:
mHCl=(0,2+ 0,01)x 36,5 = 10,95gam
mddHCl=10.95x100/7.3=150gam |
0,25
0,25
0,25
0,25
0,25
0,25
0,25
0.25
0,25
0,25 |
| Câu 3: 1,5đ |
Gọi x, y lần lượt là số mol của Al, Mg.
nH2= =0,07 mol =0,07 mol
- Thí nghiệm 1 : phản ứng:
2 Al + 3 H2SO4 → Al2(SO4)3 + 3 H2
x mol 3/2x mol
Mg + H2SO4 → Mg SO4 + H2
y mol y mol
- Thí nghiệm 2 : có phản ứng:
2 Al + 2 NaOH + 2 H2O → 2 NaAlO2 + 3 H2
Chất rắn còn lại sau tn 2 là Mg nên mMg = 0,6 g.
Ta có y =  = 0,025 mol → 3/2x + 0,025 = 0,07 = 0,025 mol → 3/2x + 0,025 = 0,07
→ x = 0,03 mol → mAl = 0,03. 27 = 0,81 g
Mhh A = 0,81 + 0,6 = 1,41 g
% Al =  100% = 57,4 % → %Mg = 100 – 57,4 = 42,6%. 100% = 57,4 % → %Mg = 100 – 57,4 = 42,6%. |
0,25
0,25
0,25
0,25
0,25
0,25 |