Giải bài tập Hóa học 9, Bài 29: Axit cacbonic và muối cacbonat
2019-07-02T04:38:38-04:00
2019-07-02T04:38:38-04:00
Giải bài tập Hóa học 9, Bài 29: Axit cacbonic và muối cacbonat
/themes/cafe/images/no_image.gif
Bài Kiểm Tra
https://baikiemtra.com/uploads/bai-kiem-tra-logo.png
Thứ ba - 02/07/2019 04:38
Giải bài tập Hóa học 9, Bài 29: Axit cacbonic và muối cacbonat
Bài 1. Hãy lấy thí dụ chứng tỏ rằng H2CO3 là axit yếu hơn HCl và là axit không bền. Viết phương trình hóa học.
Hướng dẫn giải:
Thí dụ chứng tỏ rằng H2CO3 là axit yếu hơn HCl và là axit không bền.
2HCl + CaCO3 → CaCl2 + H2CO3
H2CO3 → H2O + CO2↑
Bài 2. Dựa vào tính chất hóa học của muối cacbonat, hãy nêu tính chét của muối MgCO3 và viết các phương trình hóa học minh họa.
Hướng dẫn giải:
a) Tác dụng với dung dịch axit
MgCO3 + 2HCl → MgCl2 + H2O + CO2↑
b) Tác dụng bởi nhiệt
MgCO3 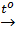 MgO + CO2↑
Bài 3. Viết các phương trình hóa học biểu diễn chuyển hóa sau:
C
MgO + CO2↑
Bài 3. Viết các phương trình hóa học biểu diễn chuyển hóa sau:
C 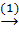 CO2
CO2 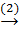 CaCO3
CaCO3 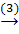 CO2
Hướng dẫn giải:
C + O2 → CO2 (1)
CO2 + Ca(OH)2 → CaCO3↓ + H2O (2)
CaCO3
CO2
Hướng dẫn giải:
C + O2 → CO2 (1)
CO2 + Ca(OH)2 → CaCO3↓ + H2O (2)
CaCO3 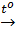 CaO + CO2↑ (3)
Bài 4. Hãy cho biết trong các cặp chất sau đây, cặp nào có thể tác dụng với nhau?
a) H2SO4 và KHCO3; d) CaCl2 và Na2CO3
b) K2CO3 và NaCl; e) Ba(OH)2 và K2CO3
c) MgCO3 và HCl;
Giải thích và viết các phương trình hóa học.
Hướng dẫn giải:
CaO + CO2↑ (3)
Bài 4. Hãy cho biết trong các cặp chất sau đây, cặp nào có thể tác dụng với nhau?
a) H2SO4 và KHCO3; d) CaCl2 và Na2CO3
b) K2CO3 và NaCl; e) Ba(OH)2 và K2CO3
c) MgCO3 và HCl;
Giải thích và viết các phương trình hóa học.
Hướng dẫn giải:
| Cặp chất |
Phương trình hóa học |
| a) H2SO4 và KHCO3 |
H2SO4 + 2KHCO3 → 2CO2↑ + K2SO4 + 2H2O |
| b) K2CO3 và NaCl |
Không phản ứng vì không tạo chất rắn (↓) khí (↑) |
| c) MgCO3 và HCl |
MgCO3 + 2HCl → MgCl2 + H2O + CO2(khí) |
| d) CaCl2 và Na2CO3 |
CaCl2 + Na2CO3 → CaCO3(rắn) + 2NaCl |
| e) Ba(OH)2 và K2CO3 |
Ba(OH)2 + K2CO3 → BaCO3(rắn) + 2KOH |
Bài 5. Hãy tính thể tích khí CO2 (đktc) tạo thành để dập tắt đám cháy nếu trong bình chữa cháy có dung dịch chứa 980g H2SO4 tác dụng với dung dịch NaHCO3
Hướng dẫn giải:
H2SO4 + NaHCO3 → NaHSO4 + H2O + CO2↑
1mol 1mol = 22,4 lít
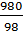 = 10 mol 10 x 22,4 = 224 lít
Thể tích CO2 tạo thành ở đktc là 224 lít.
= 10 mol 10 x 22,4 = 224 lít
Thể tích CO2 tạo thành ở đktc là 224 lít.
© Bản quyền thuộc về
Bài kiểm tra. Ghi rõ nguồn Bài kiểm tra.com khi sao chép nội dung này.