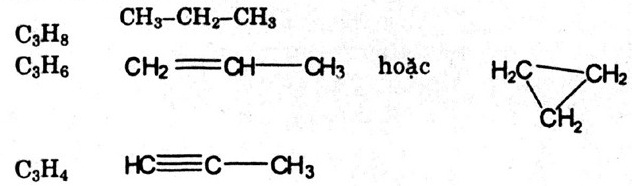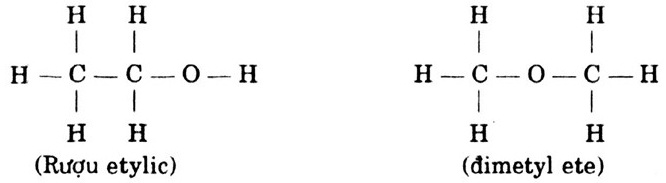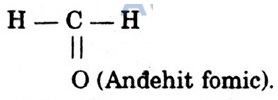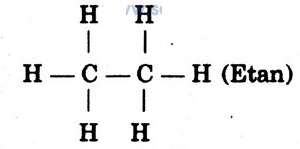Giải bài tập Hóa học 9, Bài 42: Luyện tập chương 4: Hiđrocacbon – nhiên liệu
2019-07-04T05:34:45-04:00
2019-07-04T05:34:45-04:00
Giải bài tập Hóa học 9, Bài 42: Luyện tập chương 4: Hiđrocacbon – nhiên liệu
/themes/cafe/images/no_image.gif
Bài Kiểm Tra
https://baikiemtra.com/uploads/bai-kiem-tra-logo.png
Thứ năm - 04/07/2019 05:29
Giải bài tập Hóa học 9, Bài 42: Luyện tập chương 4: Hiđrocacbon – nhiên liệu
Bài 1. Viết công thức cấu tạo đầy đủ và thu gọn của các chất hữu cơ có công thức phân tử sau: C3H8; C3H6; C3H4
Hướng dẫn giải:
Công thức cấu tạo thu gọn:
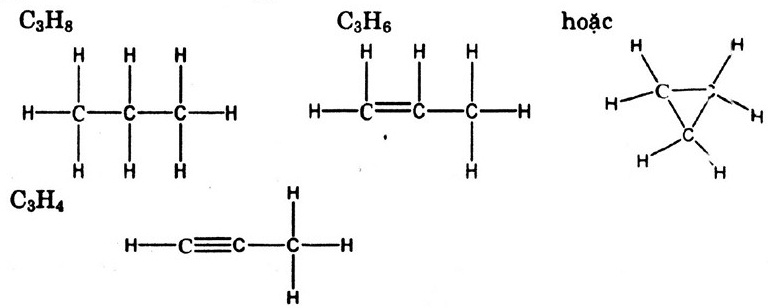
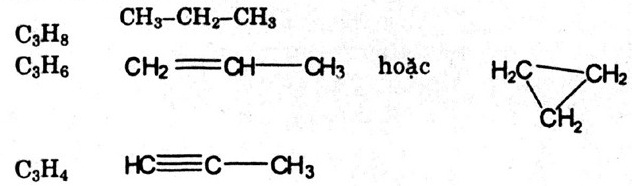 Công thức cấu tạo đầy đủ:
Công thức cấu tạo đầy đủ:
 Bài 2. Có hai bình đựng hai chất khí là CH4, C2H4. Chỉ dùng cung dịch brom có thể phân biệt được hai chất khí trên không? Nêu cách tiến hành.
Hướng dẫn giải:
Sục từng khí vào ống nghiệm dựng dung dịch brom, nếu màu nâu đỏ của dung dịch biến mất thì đó là khí C2H4. Chất không làm mất màu dung dịch brom là CH4.
Bài 3. Biết 0,01 mol hiđrocacbon X có thể tác dụng tối đa với l00ml dung dịch brom 0,1M. Vậy X là hiđrocacbon nào trong số các chất sau?
a) CH4; b) C2H2; c) C2H4 d) C6H6
Hướng dẫn giải:
Trong 4 hiđrocacbon trên, có hai chất CH4 và C6H6 không làm mất màu dung dịch brom. Như vậy chỉ còn lựa chọn giữa phương án b: C2H2 và c: C2H4
Nhận xét: C2H4 có một liên kết đôi cho nên số mol brom tối đa mà chất này tác dụng bằng số mol của nó. Trong khi C2H2 có một liên kết 3 cho nên số mol brom tối đa mà chất này tác dụng bằng hai lần số mol của C2H2.
Theo bài ra, số mol hiđrocacbon = 0,01 = số mol brom = 0,1 x 0,1
Ta kết luận phương án c: C2H4 là đúng.
Bài 4. Đốt cháy 3 gam chất hữu cơ A, thu được 8,8 gam khí CO2 và 5,4 gam H2O.
a) Trong chất hữu cơ A có những nguyên tố nào?
b) Biết phân tử khối của A nhỏ hơn 40. Tìm công thức phân tử của A.
c) Chất A có làm mất màu dung dịch brom không?
d) Viết phương trình hóa học của A với clo khi có ánh sáng.
Hướng dẫn giải:
a) Trong chất hữu cơ A có những nguyên tố nào?
Khi đốt cháy chất hữu cơ, toàn bộ C sẽ chuyển thành CO2 và toàn bộ H sẽ chuyển thành H2O. Nếu tổng khối lượng của C và H bằng klối lượng chất hữu cơ đem đốt ta kết luận thành phần phân tử chỉ có c và H. Nếu tổng này nhỏ hơn thì phần còn lại là O.
Khối lương C =
Bài 2. Có hai bình đựng hai chất khí là CH4, C2H4. Chỉ dùng cung dịch brom có thể phân biệt được hai chất khí trên không? Nêu cách tiến hành.
Hướng dẫn giải:
Sục từng khí vào ống nghiệm dựng dung dịch brom, nếu màu nâu đỏ của dung dịch biến mất thì đó là khí C2H4. Chất không làm mất màu dung dịch brom là CH4.
Bài 3. Biết 0,01 mol hiđrocacbon X có thể tác dụng tối đa với l00ml dung dịch brom 0,1M. Vậy X là hiđrocacbon nào trong số các chất sau?
a) CH4; b) C2H2; c) C2H4 d) C6H6
Hướng dẫn giải:
Trong 4 hiđrocacbon trên, có hai chất CH4 và C6H6 không làm mất màu dung dịch brom. Như vậy chỉ còn lựa chọn giữa phương án b: C2H2 và c: C2H4
Nhận xét: C2H4 có một liên kết đôi cho nên số mol brom tối đa mà chất này tác dụng bằng số mol của nó. Trong khi C2H2 có một liên kết 3 cho nên số mol brom tối đa mà chất này tác dụng bằng hai lần số mol của C2H2.
Theo bài ra, số mol hiđrocacbon = 0,01 = số mol brom = 0,1 x 0,1
Ta kết luận phương án c: C2H4 là đúng.
Bài 4. Đốt cháy 3 gam chất hữu cơ A, thu được 8,8 gam khí CO2 và 5,4 gam H2O.
a) Trong chất hữu cơ A có những nguyên tố nào?
b) Biết phân tử khối của A nhỏ hơn 40. Tìm công thức phân tử của A.
c) Chất A có làm mất màu dung dịch brom không?
d) Viết phương trình hóa học của A với clo khi có ánh sáng.
Hướng dẫn giải:
a) Trong chất hữu cơ A có những nguyên tố nào?
Khi đốt cháy chất hữu cơ, toàn bộ C sẽ chuyển thành CO2 và toàn bộ H sẽ chuyển thành H2O. Nếu tổng khối lượng của C và H bằng klối lượng chất hữu cơ đem đốt ta kết luận thành phần phân tử chỉ có c và H. Nếu tổng này nhỏ hơn thì phần còn lại là O.
Khối lương C = 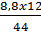 = 2,4 (g); Khối lượng H =
= 2,4 (g); Khối lượng H = 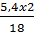 = 0,6 (g)
mC + mH = 2,4 + 0,6 = 3,0 ⇒ A chỉ gồm C và H.
b) Biết phân tử khối của A nhỏ hơn 40. Tìm công thức phân tử của A.
Cách 1: Biện luận MA < 40 cho nên số mol C lớn nhất có thể là 2.
Mặt khác do sản phẩm cháy có số mol CO2 = 0,2 < số mol H2O = 0,3 cho nên A là hiđrocacbon no
A là C2H6 ⇒ MA = 24 + 6 = 30
Cách 2: Đặt công thức phân tử của A là CxHy theo tính toán ở phần a ta có tỷ lệ:
x : y =
= 0,6 (g)
mC + mH = 2,4 + 0,6 = 3,0 ⇒ A chỉ gồm C và H.
b) Biết phân tử khối của A nhỏ hơn 40. Tìm công thức phân tử của A.
Cách 1: Biện luận MA < 40 cho nên số mol C lớn nhất có thể là 2.
Mặt khác do sản phẩm cháy có số mol CO2 = 0,2 < số mol H2O = 0,3 cho nên A là hiđrocacbon no
A là C2H6 ⇒ MA = 24 + 6 = 30
Cách 2: Đặt công thức phân tử của A là CxHy theo tính toán ở phần a ta có tỷ lệ:
x : y = 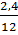 :
: 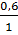 = 2 : 6 = 1 : 3
Công thức đơn giản nhất của A là CH3
Công thức phân tử là (CH3)n với MA < 40 thì n = 2
Công thức phân tử của A là C2H6 ⇒ MA = 24 + 6 = 30
c) Chất A có làm mất màu dung dịch brom không?
A là hiđrocacbon no cho nên không làm mất màu dung dịch brom.
d) Viết phương trình hóa học của A với clo khi có ánh sáng.
C2H6 + Cl2
= 2 : 6 = 1 : 3
Công thức đơn giản nhất của A là CH3
Công thức phân tử là (CH3)n với MA < 40 thì n = 2
Công thức phân tử của A là C2H6 ⇒ MA = 24 + 6 = 30
c) Chất A có làm mất màu dung dịch brom không?
A là hiđrocacbon no cho nên không làm mất màu dung dịch brom.
d) Viết phương trình hóa học của A với clo khi có ánh sáng.
C2H6 + Cl2 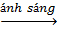 C2H5Cl + HCl
C. BÀI TẬP BỔ SUNG
Bài 1. Hãy so sánh % khối lượng của cacbon trong các chất sau: C2H6, C2H5Cl, C2H4Cl2, C2H3Cl3.
Hướng dẫn giải:
% về khối lượng:
%C(C2H6) =
C2H5Cl + HCl
C. BÀI TẬP BỔ SUNG
Bài 1. Hãy so sánh % khối lượng của cacbon trong các chất sau: C2H6, C2H5Cl, C2H4Cl2, C2H3Cl3.
Hướng dẫn giải:
% về khối lượng:
%C(C2H6) = 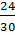 x 100 = 80%
%C(C2H5Cl) =
x 100 = 80%
%C(C2H5Cl) = 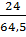 x 100 = 37,2%
%C(C2H4Cl2) =
x 100 = 37,2%
%C(C2H4Cl2) = 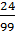 x 100% = 24,24%
%C(C2H3Cl3) =
x 100% = 24,24%
%C(C2H3Cl3) = 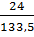 ≈ 17,89%
Vậy %C(C2H6) > %C(C2H5Cl) > %C(C2H4Cl2) > %C(C2H3Cl3)
Nhận xét: Khối lượng C trong các hợp chất là khống đổi. Khối lượng phân tử càng lớn thì %C trong phân tử càng nhỏ. Khi thay thế nguyên tử H trong phân tử bằng các nguyên tử Cl, khối lượng phân tử tăng lên vì vậy %C càng nhỏ.
Bài 2. Rượu etylic có công thức C2H6O. Hãy tính thành phần phần trăm khối lượng của các nguyên tố trong rượu axetic.
Hướng dẫn giải:
≈ 17,89%
Vậy %C(C2H6) > %C(C2H5Cl) > %C(C2H4Cl2) > %C(C2H3Cl3)
Nhận xét: Khối lượng C trong các hợp chất là khống đổi. Khối lượng phân tử càng lớn thì %C trong phân tử càng nhỏ. Khi thay thế nguyên tử H trong phân tử bằng các nguyên tử Cl, khối lượng phân tử tăng lên vì vậy %C càng nhỏ.
Bài 2. Rượu etylic có công thức C2H6O. Hãy tính thành phần phần trăm khối lượng của các nguyên tố trong rượu axetic.
Hướng dẫn giải:
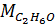 = 46
%C =
= 46
%C = 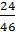 x 100 = 52,17%
%O =
x 100 = 52,17%
%O = 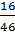 x 100 = 34,78%
%H = (100 - 52,17 - 34,78)% = 13,05%
Bài 3. Phân tử hợp chất hữu cơ A chỉ chứa C và H. Khi đốt cháy 9 gam chất A thu được 16,2 gam H2O. Hãy xác định công thức phân tử của A, tỉ khối hơi của A so với H2 là 15.
Hướng dẫn giải:
Khối lượng của H trong 16,2 g H2O là:
mH =
x 100 = 34,78%
%H = (100 - 52,17 - 34,78)% = 13,05%
Bài 3. Phân tử hợp chất hữu cơ A chỉ chứa C và H. Khi đốt cháy 9 gam chất A thu được 16,2 gam H2O. Hãy xác định công thức phân tử của A, tỉ khối hơi của A so với H2 là 15.
Hướng dẫn giải:
Khối lượng của H trong 16,2 g H2O là:
mH = 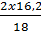 = 1,8 g
Khối lượng C trong A là: mC = 9 - 1,8 = 7,2g
CTPT A có dạng CxHy: M = 15 . 2 = 30
Ta có:
= 1,8 g
Khối lượng C trong A là: mC = 9 - 1,8 = 7,2g
CTPT A có dạng CxHy: M = 15 . 2 = 30
Ta có: 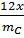 =
= 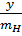 =
=  ⇒ x =
⇒ x =  = 2; y =
= 2; y = 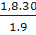 = 6
Vậy CTPT của A là C2H6.
Bài 4. Khi phân tích 2,3 gam một hợp chất hữu cơ A, thấy có 1,2g C, 0,3 g H và 0,8(g)O. Hãy xác định:
a) Tính % khối lượng các nguyên tố trong hữu cơ A
b) CTPT của A biết tỉ khối của A đối với H2 là 23.
c) CTCT của A.
Hướng dẫn giải:
%C =
= 6
Vậy CTPT của A là C2H6.
Bài 4. Khi phân tích 2,3 gam một hợp chất hữu cơ A, thấy có 1,2g C, 0,3 g H và 0,8(g)O. Hãy xác định:
a) Tính % khối lượng các nguyên tố trong hữu cơ A
b) CTPT của A biết tỉ khối của A đối với H2 là 23.
c) CTCT của A.
Hướng dẫn giải:
%C = 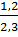 x 100 ≈ 52,17%
%H =
x 100 ≈ 52,17%
%H = 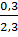 x 100 ≈ 13,04%
%O =
x 100 ≈ 13,04%
%O = 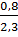 x 100 ≈ 34,79%
b) Khối lượng mol của A: M = 23. 2 = 46(g)
Đặt công thức của A là CxHyOz, ta có tỉ lệ:
x 100 ≈ 34,79%
b) Khối lượng mol của A: M = 23. 2 = 46(g)
Đặt công thức của A là CxHyOz, ta có tỉ lệ:
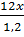 =
= 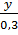 =
= 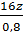 =
= 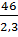 Giải ra, ta được: x = 2, y = 6, z = 1. Vậy CTPT của A là: C2H6O
c) A có 2 cấu tạo:
Giải ra, ta được: x = 2, y = 6, z = 1. Vậy CTPT của A là: C2H6O
c) A có 2 cấu tạo:
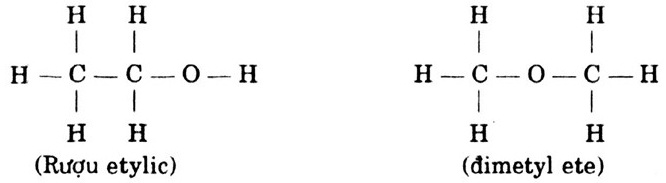 Bài 5. Một hợp chất hữu cơ A có chứa 40%C; 6,67%H và 53,33% O về khối lượng. Hãy xác định:
a) CTPT của A biết tỉ khối hơi của A so với H2 là 15.
b) CTCT của A.
Hướng dẫn giải:
a) 100g A có mC = 40; mH = 6,67 và mO = 53,33
- Khối lượng mol của A: M = 15.2 = 30
- Đặt CT của A: CxHyOz, ta có tỉ lệ:
Bài 5. Một hợp chất hữu cơ A có chứa 40%C; 6,67%H và 53,33% O về khối lượng. Hãy xác định:
a) CTPT của A biết tỉ khối hơi của A so với H2 là 15.
b) CTCT của A.
Hướng dẫn giải:
a) 100g A có mC = 40; mH = 6,67 và mO = 53,33
- Khối lượng mol của A: M = 15.2 = 30
- Đặt CT của A: CxHyOz, ta có tỉ lệ:
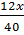 =
= 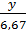 =
= 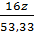 =
= 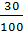 Giải ra ta được x = 1, y = 2, z = 1. Vậy CTPT của A là: CH2O
b) A có cấu tạo:
Giải ra ta được x = 1, y = 2, z = 1. Vậy CTPT của A là: CH2O
b) A có cấu tạo:
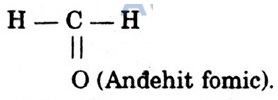 Bài 6. Đốt cháy hoàn toàn 6,2 gam một hợp chất A chứa (C, H, N); thu được nước, 8,8 gam CO2 và 2,24 lít N2 (đktc) . Hãy xác định:
a) CTPT của A biết M = 31
b) CTCT của A biết trong hợp chất nitơ có hóa trị (III).
Hướng dẫn giải:
a) Lượng C, H, N trong 6,2 gam A
Bài 6. Đốt cháy hoàn toàn 6,2 gam một hợp chất A chứa (C, H, N); thu được nước, 8,8 gam CO2 và 2,24 lít N2 (đktc) . Hãy xác định:
a) CTPT của A biết M = 31
b) CTCT của A biết trong hợp chất nitơ có hóa trị (III).
Hướng dẫn giải:
a) Lượng C, H, N trong 6,2 gam A
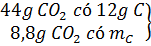 → mC =
→ mC = 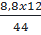 = 2,4
= 2,4
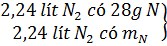 → mN =
→ mN = 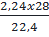 = 2,8
+ mH = 6,2 – mC – mN = 1,0 (gam)
- Đặt CT của A là CxHyNz ta có tỉ lệ:
= 2,8
+ mH = 6,2 – mC – mN = 1,0 (gam)
- Đặt CT của A là CxHyNz ta có tỉ lệ:
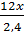 =
=  =
= 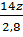 =
= 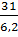 Giải ra ta được x= 1; y= 5; z = 1. Vậy CTPT của A là: CH5N.
b) A có cấu tạo:
Giải ra ta được x= 1; y= 5; z = 1. Vậy CTPT của A là: CH5N.
b) A có cấu tạo:
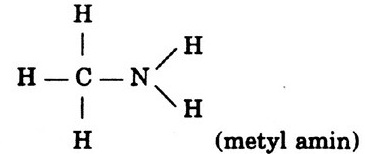 Bài 7. Đốt cháy hoàn toàn 100ml hợp chất hữu cơ chứa 2 nguyên tố, cần 350ml O2 và thu được 200ml CO2. Xác định CTPT và CTCT của hợp chất biết các thể tích đều được đo ở cùng điều kiện.
Hướng dẫn giải:
- Hợp chất hữu cơ chứa 2 nguyên tố phải có cacbon, nguyên tố thứ hai chỉ có thể là hiđro. Công thức có dạng CxHy
- Phương trình phản ứng cháy:
CxHy + (x +
Bài 7. Đốt cháy hoàn toàn 100ml hợp chất hữu cơ chứa 2 nguyên tố, cần 350ml O2 và thu được 200ml CO2. Xác định CTPT và CTCT của hợp chất biết các thể tích đều được đo ở cùng điều kiện.
Hướng dẫn giải:
- Hợp chất hữu cơ chứa 2 nguyên tố phải có cacbon, nguyên tố thứ hai chỉ có thể là hiđro. Công thức có dạng CxHy
- Phương trình phản ứng cháy:
CxHy + (x +  ) O2 → xCO2 +
) O2 → xCO2 +  H2O
1 … (x +
H2O
1 … (x +  ) …… x(ml)
100 .... .. 350 ……… 200 (ml)
Ta có tỉ lệ:
) …… x(ml)
100 .... .. 350 ……… 200 (ml)
Ta có tỉ lệ: 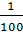 =
= 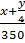 =
= 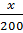 Giải ra, ta được x = 2, y = 6. CTPT: C2H6.
Có cấu tạo:
Giải ra, ta được x = 2, y = 6. CTPT: C2H6.
Có cấu tạo:
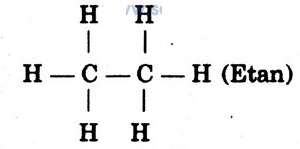 Bài 8. Một hợp chất hữu cơ 2 nguyên tố cố khối lượng mol bằng 30. Biết trong hợp chất hữu cơ, nguyên tử của nguyên tố cacbon luôn có hóa trị (IV). Biện luận tìm công thức.
Hướng dẫn giải:
- CTPT của hợp chất hữu cơ có dạng CxHy
- Ta có khối lượng mol của hợp chất:
M = 12x + y = 30
Hay: y = 30 - 12x
x, y nguyên dương:
x = 1 → y = 18: không có CT phù hợp
x = 2 → y = 6: C2H6: phù hợp
x
Bài 8. Một hợp chất hữu cơ 2 nguyên tố cố khối lượng mol bằng 30. Biết trong hợp chất hữu cơ, nguyên tử của nguyên tố cacbon luôn có hóa trị (IV). Biện luận tìm công thức.
Hướng dẫn giải:
- CTPT của hợp chất hữu cơ có dạng CxHy
- Ta có khối lượng mol của hợp chất:
M = 12x + y = 30
Hay: y = 30 - 12x
x, y nguyên dương:
x = 1 → y = 18: không có CT phù hợp
x = 2 → y = 6: C2H6: phù hợp
x 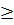 3 → y < 0 loại. Vậy CTPT của hợp chất là C2H6.
Bài 9. Để đốt cháy 4,48 lít khí metan cần phải dùng:
a) Bao nhiêu lít oxi?
b) Bao nhiêu lít không khí chứa 20% thể tích khí oxi?
Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
Hướng dẫn giải:
Số mol metan: n = 4,48 : 22,4 = 0,2mol
PTPƯ: CH4 + 2O2 → CO2↑ + 2H2O
0,2 … 0,4 mol
a) Thể tích oxi cần: V = 0,4.22,4 = 8,96 (l)
b) Thể tích không khí: V = 8,96 . 100 : 20 = 44,8 (l)
Bài 10. Biết rằng 0,224 lít khí etilen (đktc) làm mất màu 50ml dung dịch brom.
a) Tính nồng độ CM của dung dịch brom.
b) Nếu cũng dùng dung dịch brom trên thì làm mất màu bao nhiêu ml axetilen(đktc).
Hướng dẫn giải:
a) C2H4 + Br2 → C2H4Br2
0,01 … 0,01 mol
Nồng độ dung dịch Br2: CM = 0,01 : 0,05 = 0,2M
b) Axetilen tác dụng với Br2, cần gấp đôi lượng Br2 so với etilen. Vì vậy cùng thể tích Br2 thì làm mất màu hết 0,224 : 2 = 0,112 lit axetilen.
Bài 11. Viết phương trình hóa học (có ghi rõ điều kiện phản ứng) khi cho benzen tác dụng dung dịch Br2. Tính khối lượng benzen cần dùng để điều chế 31,4 gam brombenzen. Biết hiệu suất phản ứng đạt 60%.
Hướng dẫn giải:
a) Phương trình hóa học:
3 → y < 0 loại. Vậy CTPT của hợp chất là C2H6.
Bài 9. Để đốt cháy 4,48 lít khí metan cần phải dùng:
a) Bao nhiêu lít oxi?
b) Bao nhiêu lít không khí chứa 20% thể tích khí oxi?
Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
Hướng dẫn giải:
Số mol metan: n = 4,48 : 22,4 = 0,2mol
PTPƯ: CH4 + 2O2 → CO2↑ + 2H2O
0,2 … 0,4 mol
a) Thể tích oxi cần: V = 0,4.22,4 = 8,96 (l)
b) Thể tích không khí: V = 8,96 . 100 : 20 = 44,8 (l)
Bài 10. Biết rằng 0,224 lít khí etilen (đktc) làm mất màu 50ml dung dịch brom.
a) Tính nồng độ CM của dung dịch brom.
b) Nếu cũng dùng dung dịch brom trên thì làm mất màu bao nhiêu ml axetilen(đktc).
Hướng dẫn giải:
a) C2H4 + Br2 → C2H4Br2
0,01 … 0,01 mol
Nồng độ dung dịch Br2: CM = 0,01 : 0,05 = 0,2M
b) Axetilen tác dụng với Br2, cần gấp đôi lượng Br2 so với etilen. Vì vậy cùng thể tích Br2 thì làm mất màu hết 0,224 : 2 = 0,112 lit axetilen.
Bài 11. Viết phương trình hóa học (có ghi rõ điều kiện phản ứng) khi cho benzen tác dụng dung dịch Br2. Tính khối lượng benzen cần dùng để điều chế 31,4 gam brombenzen. Biết hiệu suất phản ứng đạt 60%.
Hướng dẫn giải:
a) Phương trình hóa học:
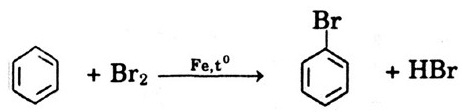 b) 78 …………….....................157g
m …………...........................31,4g
Vì H = 60% nên khối lương benzen cần: m =
b) 78 …………….....................157g
m …………...........................31,4g
Vì H = 60% nên khối lương benzen cần: m = 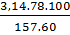 = 26 g
Bài 12. Hãy cho biết chất nào trong các chất sau đây có thể làm mất màu dung dịch brom. Giải thích và viết phương trình hóa học (nếu có).
CH2 = CH2 ; CH3 - CH = CH2 ; CH
= 26 g
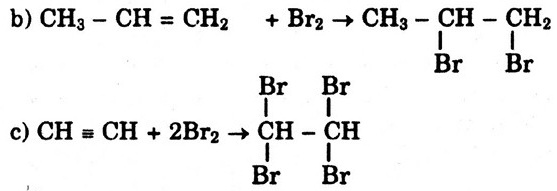
Bài 12. Hãy cho biết chất nào trong các chất sau đây có thể làm mất màu dung dịch brom. Giải thích và viết phương trình hóa học (nếu có).
CH2 = CH2 ; CH3 - CH = CH2 ; CH 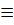 CH ; CH3 – CH3 ; CH4
A B C D E
Hướng dẫn giải:
Các chất làm mất màu dung dịch Br2 là: A, B và C
Các phương trình phản ứng :
a) CH2 = CH2 + Br2 → CH2Br – CH2Br
CH ; CH3 – CH3 ; CH4
A B C D E
Hướng dẫn giải:
Các chất làm mất màu dung dịch Br2 là: A, B và C
Các phương trình phản ứng :
a) CH2 = CH2 + Br2 → CH2Br – CH2Br
 Bài 13. Đốt cháy 6 gam chất hữu cơ A, thu được 17,6 gam khí CO2 và 10,8 gam H2O.
a) Trong chất A có những nguyên tố nào?
b) Tìm công thức phân tử của A. Biết MA= 30.
c) Viết phương trình hóa học của A với clo khi có ánh sáng.
Hướng dẫn giải:
a) mH = 2 . 10,8 : 18 = 1,2g
mC = 12 . 17,6 : 44 = 4,8g
mO = 6 - 1,2 - 4,8 = 0. Vậy trong A có C và H.
b) Gọi CTPT của A là CxHy có M = 30
Ta có:
Bài 13. Đốt cháy 6 gam chất hữu cơ A, thu được 17,6 gam khí CO2 và 10,8 gam H2O.
a) Trong chất A có những nguyên tố nào?
b) Tìm công thức phân tử của A. Biết MA= 30.
c) Viết phương trình hóa học của A với clo khi có ánh sáng.
Hướng dẫn giải:
a) mH = 2 . 10,8 : 18 = 1,2g
mC = 12 . 17,6 : 44 = 4,8g
mO = 6 - 1,2 - 4,8 = 0. Vậy trong A có C và H.
b) Gọi CTPT của A là CxHy có M = 30
Ta có: 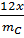 =
= 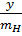 =
=  ⇒ x =
⇒ x = 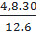 = 2; y =
= 2; y = 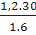 = 6
Vậy CTPT của A là C2H6
c) Tác dụng với clo: C2H6 + Cl2 → C2H5Cl + HCl
Bài 14. Đốt cháy hoàn toàn 1,6 gam một hiđrocacbon A. Toàn bộ sản phẩm cháy được dẫn vào bình chứa dung dịch Ca(OH)2 dư, thấy tạo thành 10g kết tủa. Xác định tên chất A. Biết CTPT của A trùng với CT đơn giản nhất.
Hướng dẫn giải:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,1 <-----------
= 6
Vậy CTPT của A là C2H6
c) Tác dụng với clo: C2H6 + Cl2 → C2H5Cl + HCl
Bài 14. Đốt cháy hoàn toàn 1,6 gam một hiđrocacbon A. Toàn bộ sản phẩm cháy được dẫn vào bình chứa dung dịch Ca(OH)2 dư, thấy tạo thành 10g kết tủa. Xác định tên chất A. Biết CTPT của A trùng với CT đơn giản nhất.
Hướng dẫn giải:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,1 <----------- 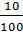 = 0,1mol
nC =
= 0,1mol
nC = 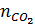 =
= 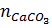 = 0,1
mC = 12 . 0,1 = 1,2 (g)
mH = 1,6 - 1,2 = 0,4 (g)
A có dạng CxHy, ta có tỉ lệ:
= 0,1
mC = 12 . 0,1 = 1,2 (g)
mH = 1,6 - 1,2 = 0,4 (g)
A có dạng CxHy, ta có tỉ lệ:
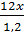 =
= 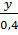 =
= 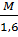 Vì không biết M, nên ta biến đổi tỉ lệ thức:
x : y =
Vì không biết M, nên ta biến đổi tỉ lệ thức:
x : y = 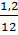 :
: 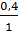 = 0,1 : 0,4 = 1 : 4.
Vậy CTPT của A là CH4 (Metan)
Bài 15. Khi cho một hiđrocacbon A tác dụng với clo trong những điều kiện thích hợp. người ta thu được sản phẩm B chứa một nguyên tử clo có tỉ khối hơi đối với hidro là 25,25. Xác định CTPT của A. Viết phương trình phản ứng.
Hướng dẫn giải:
- MB = 25,25.2 = 50,5 (g)
- CTPT của B có dạng CxHyCl (x, y nguyên dương),
ta có MB = 12x + y + 35,5 = 50,5
Hay: V = 15 - 12x
x = 1 → y = 3 → CTPT của B: CH3Cl
CTPT của A: CH4
Phương trình phản ứng:
CH4 + Cl2
= 0,1 : 0,4 = 1 : 4.
Vậy CTPT của A là CH4 (Metan)
Bài 15. Khi cho một hiđrocacbon A tác dụng với clo trong những điều kiện thích hợp. người ta thu được sản phẩm B chứa một nguyên tử clo có tỉ khối hơi đối với hidro là 25,25. Xác định CTPT của A. Viết phương trình phản ứng.
Hướng dẫn giải:
- MB = 25,25.2 = 50,5 (g)
- CTPT của B có dạng CxHyCl (x, y nguyên dương),
ta có MB = 12x + y + 35,5 = 50,5
Hay: V = 15 - 12x
x = 1 → y = 3 → CTPT của B: CH3Cl
CTPT của A: CH4
Phương trình phản ứng:
CH4 + Cl2 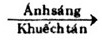 CH3Cl + HCl
(metan) (metyl clorua).
Bài 16. Người ta điều chế muội than và hiđro bằng cách nhiệt phân metan. Hỏi, nếu dùng 560 lít metan thì điều chế được bao nhiêu gam than và bao nhiêu lít H2 (các thể tích được đo ở đktc).
Hướng dẫn giải:
CH3Cl + HCl
(metan) (metyl clorua).
Bài 16. Người ta điều chế muội than và hiđro bằng cách nhiệt phân metan. Hỏi, nếu dùng 560 lít metan thì điều chế được bao nhiêu gam than và bao nhiêu lít H2 (các thể tích được đo ở đktc).
Hướng dẫn giải:
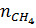 =
= 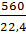 = 25 (mol)
- Phương trình phản ứng:
CH4
= 25 (mol)
- Phương trình phản ứng:
CH4 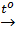 C + 2H2↑
25 25 2 . 25 = 50
mC = 12 . 25 = 300 (gam)
C + 2H2↑
25 25 2 . 25 = 50
mC = 12 . 25 = 300 (gam)
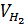 = 22,4 x 50 = 1120 (lít).
Bài 17. Đốt cháy hoàn toàn 3,8 gam hỗn hợp A gồm CH4 và co thu được 4,48 lít CO2. Hãy tính:
a) Thành phần % theo thể tích các chất trong hỗn hợp A (biết các thể tích đều được đo ở đktc).
b) VO cần dùng cho phản ứng cháy.
Hướng dẫn giải:
a) Phương trình phản ứng:
CH4 + 2O2 → CO2↑ + 2H2O
x 2x x (mol)
2CO + O2 → 2CO2
y 0,5y y (mol)
Gọi x, y là số mol CH4 và CO trong 3,8 g A. Theo giả thuyết ta có:
mA = 16x + 28y = 3,8 (1)
= 22,4 x 50 = 1120 (lít).
Bài 17. Đốt cháy hoàn toàn 3,8 gam hỗn hợp A gồm CH4 và co thu được 4,48 lít CO2. Hãy tính:
a) Thành phần % theo thể tích các chất trong hỗn hợp A (biết các thể tích đều được đo ở đktc).
b) VO cần dùng cho phản ứng cháy.
Hướng dẫn giải:
a) Phương trình phản ứng:
CH4 + 2O2 → CO2↑ + 2H2O
x 2x x (mol)
2CO + O2 → 2CO2
y 0,5y y (mol)
Gọi x, y là số mol CH4 và CO trong 3,8 g A. Theo giả thuyết ta có:
mA = 16x + 28y = 3,8 (1)
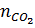 = x + y =
= x + y = 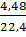 = 0,2 (2)
Giải hệ ta được: x = 0,15 mol CH4;
y = 0,05 mol CO
%CH4 =
= 0,2 (2)
Giải hệ ta được: x = 0,15 mol CH4;
y = 0,05 mol CO
%CH4 = 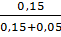 x 100 = 75%
%CO =
x 100 = 75%
%CO = 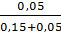 x 100 = 25%
b)
x 100 = 25%
b) 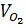 = 22,4(2x + 0,5y) = 22,4 . 0,325 = 7,28 (lít)
Bài 18. Cho một luồng khí hiđrocacbon lội qua dung dịch nước brom lấy dư, thu được sản phẩm chứa 2 nguyên tử brom, trong đó brom chiếm 85,1% về khối lượng. Xác định CT của hiđrocacbon, viết phương trình phản ứng.
Hướng dẫn giải:
Công thức của hợp chất chứa brom có dạng: CxHyBr2
Theo giả thiết ta có:
= 22,4(2x + 0,5y) = 22,4 . 0,325 = 7,28 (lít)
Bài 18. Cho một luồng khí hiđrocacbon lội qua dung dịch nước brom lấy dư, thu được sản phẩm chứa 2 nguyên tử brom, trong đó brom chiếm 85,1% về khối lượng. Xác định CT của hiđrocacbon, viết phương trình phản ứng.
Hướng dẫn giải:
Công thức của hợp chất chứa brom có dạng: CxHyBr2
Theo giả thiết ta có:
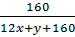 =
= 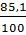 Hay: 12x + y + 160 = 160 .
Hay: 12x + y + 160 = 160 . 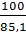 = 188
y = 28 - 12x
Để phù hợp với hóa trị của các nguyên tố chỉ có x = 2, y = 4 là phù hợp. Vậy CTPT của hiđro cacbon là C2H4 (etilen)
- Phương trình phản ứng: CH2 = CH2 + Br2 → CH2Br – CH2Br.
Bài 19. Dẫn 10 lít hỗn hợp gồm CH4 và C2H4 vào bình chứa dung dịch brom, thấy nước brom bị nhạt màu một phần và có khối lượng tăng lên 8,4 gam. Tính % V mỗi khí trong hỗn hợp. Biết các thể tích đều được đo ở đktc.
Hướng dẫn giải:
Chỉ có C2H4 phản ứng:
C2H4 + Br2 → C2H4Br2.
Độ tăng khối lượng của bình chứa brom là lượng C2H4 đã phản ứng :
= 188
y = 28 - 12x
Để phù hợp với hóa trị của các nguyên tố chỉ có x = 2, y = 4 là phù hợp. Vậy CTPT của hiđro cacbon là C2H4 (etilen)
- Phương trình phản ứng: CH2 = CH2 + Br2 → CH2Br – CH2Br.
Bài 19. Dẫn 10 lít hỗn hợp gồm CH4 và C2H4 vào bình chứa dung dịch brom, thấy nước brom bị nhạt màu một phần và có khối lượng tăng lên 8,4 gam. Tính % V mỗi khí trong hỗn hợp. Biết các thể tích đều được đo ở đktc.
Hướng dẫn giải:
Chỉ có C2H4 phản ứng:
C2H4 + Br2 → C2H4Br2.
Độ tăng khối lượng của bình chứa brom là lượng C2H4 đã phản ứng :
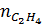 =
= 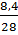 = 0,3 (mol)
= 0,3 (mol)
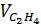 = 22,4 x 0,3 = 6,72 (lít)
%C2H4 =
= 22,4 x 0,3 = 6,72 (lít)
%C2H4 = 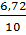 x 100 = 67,2%
%CH4 = 100 - 67,2 = 32,8% .
Bài 20. Dẫn 10 lít hỗn hợp A (đktc) gồm CH4, C2H4, CO2 lần lượt qua bình (1) chứa dung dịch Ca(OH)2 dư và bình (2) chứa dung dịch brom dư. Thấy bình (1) xuất hiện 10 gam kết tủa, bình (2) khối lượng tăng thêm 5,6 gam.
a) Viết các phương trình phản ứng.
b) Tính % V mỗi khí trong hỗn hợp A
Hướng dẫn giải:
a) Ở bình 1:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Ở bình (2)
C2H4 + Br2 → C2H4Br2
- CH4 đi qua cả hai bình và không tác dụng với Ca(OH)2 và dung dịch Br2.
b)
x 100 = 67,2%
%CH4 = 100 - 67,2 = 32,8% .
Bài 20. Dẫn 10 lít hỗn hợp A (đktc) gồm CH4, C2H4, CO2 lần lượt qua bình (1) chứa dung dịch Ca(OH)2 dư và bình (2) chứa dung dịch brom dư. Thấy bình (1) xuất hiện 10 gam kết tủa, bình (2) khối lượng tăng thêm 5,6 gam.
a) Viết các phương trình phản ứng.
b) Tính % V mỗi khí trong hỗn hợp A
Hướng dẫn giải:
a) Ở bình 1:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Ở bình (2)
C2H4 + Br2 → C2H4Br2
- CH4 đi qua cả hai bình và không tác dụng với Ca(OH)2 và dung dịch Br2.
b) 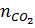 =
= 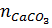 =
= 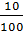 = 0,1 →
= 0,1 → 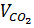 = 22,4 x 0,1 = 2,24 (l)
= 22,4 x 0,1 = 2,24 (l)
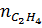 =
= 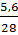 = 0,2 →
= 0,2 → 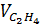 = 22,4 x 0,2 = 4,48
%CO2 =
= 22,4 x 0,2 = 4,48
%CO2 = 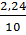 x100% = 22,4%
%C2H4 =
x100% = 22,4%
%C2H4 = 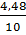 x100% = 44,8%
%CH4 = 100 – 22,4 – 44,8 = 32,8%
Bài 21. Trong phòng thí nghiệm người ta điều chế khí etilen từ rượu etylic theo phương trình:
C2H5OH
x100% = 44,8%
%CH4 = 100 – 22,4 – 44,8 = 32,8%
Bài 21. Trong phòng thí nghiệm người ta điều chế khí etilen từ rượu etylic theo phương trình:
C2H5OH 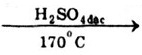 C2H4↑ + H2O
a) Hỏi nếu dùng 230ml rượu etylic có khối lượng riêng D = 0,8 g/ml thì điều chế được bao nhiêu lít etilen (ở đktc). Biết hiệu suất của phản ứng là 80%.
b) Tính lượng polietilen khi trùng hợp lượng etilen điều chế được.
Hướng dẫn giải:
a)
C2H4↑ + H2O
a) Hỏi nếu dùng 230ml rượu etylic có khối lượng riêng D = 0,8 g/ml thì điều chế được bao nhiêu lít etilen (ở đktc). Biết hiệu suất của phản ứng là 80%.
b) Tính lượng polietilen khi trùng hợp lượng etilen điều chế được.
Hướng dẫn giải:
a) 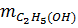 = V.D = 230 x 0,8 = 184 (gam)
- Phương trình phản ứng:
C2H5OH
= V.D = 230 x 0,8 = 184 (gam)
- Phương trình phản ứng:
C2H5OH 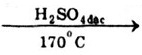 C2H4↑ + H2O
C2H4↑ + H2O
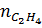 =
= 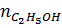 =
= 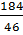 = 4 (mol)
= 4 (mol)
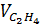 (theo lý thuyết) = 22,4 . 4 = 89,6 (lít)
(theo lý thuyết) = 22,4 . 4 = 89,6 (lít)
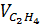 (thực tế) = 89,6 .
(thực tế) = 89,6 . 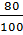 = 71,68 (lít)
b)
= 71,68 (lít)
b) 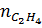 (thực tế) = 4 . 0,8 = 3,2 (mol) ⇒
(thực tế) = 4 . 0,8 = 3,2 (mol) ⇒ 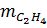 = 28 x 3,2 = 89,6 (gam)
n CH2 = CH2
= 28 x 3,2 = 89,6 (gam)
n CH2 = CH2 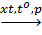 ( - CH2 = CH2 - )n
mpolietylen =
( - CH2 = CH2 - )n
mpolietylen = 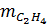 = 89,6 (gam).
Bài 22. Dẫn 0,448 lít một hiđrocacbon (đktc) vào bình chứa dung dịch brom lấy dư, thấy khối lượng bình tăng lên 0,52 gam. Hãy xác định:
a) Công thức cấu tạo của hiđrocacbon.
b) Lượng brom đã phản ứng.
Hướng dẫn giải:
a) Công thức hiđrocacbon có dạng: CxHy
m =
= 89,6 (gam).
Bài 22. Dẫn 0,448 lít một hiđrocacbon (đktc) vào bình chứa dung dịch brom lấy dư, thấy khối lượng bình tăng lên 0,52 gam. Hãy xác định:
a) Công thức cấu tạo của hiđrocacbon.
b) Lượng brom đã phản ứng.
Hướng dẫn giải:
a) Công thức hiđrocacbon có dạng: CxHy
m =  m (bình) = 0,52
m (bình) = 0,52
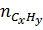 =
= 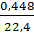 = 0,02
= 0,02
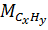 = 12x + y =
= 12x + y = 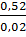 = 26
Hay y = 26 - 12x.
Để phù hợp với hóa trị của các nguyên tố chỉ có x = 2, y = 2 là phù hợp.
Vậy CTPT của hiđrocacbon là: C2H2.CTCT: H – C
= 26
Hay y = 26 - 12x.
Để phù hợp với hóa trị của các nguyên tố chỉ có x = 2, y = 2 là phù hợp.
Vậy CTPT của hiđrocacbon là: C2H2.CTCT: H – C 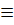 C - H (axetilen).
b) Vì brom có dư, nên ptpư: C2H2 + 2Br2 → C2H2Br4
0,02 0,04
mBr = 160 . 0,04 = 6,4 (g)
Bài 23. Hỗn hợp A gồm C2H2, H2 có tỉ khối đối với hiđro là 5. Hãy xác dnh:
a) %V mỗi khí trong hỗn hợp A.
b) Nếu đốt cháy hoàn toàn 6,72 lít hỗn hợp A (đktc) sản phẩm cháy được dẫn vào bình chứa dung dịch Ca(OH)3 dư. Hỏi khối lượng bình tăng bao nhiêu gam. Tính khối lượng kết tủa tạo thành.
Hướng dẫn giải:
a) Khối lượng của 1 mol hỗn hợp A: M = 5.2 = 10
Đặt:
C - H (axetilen).
b) Vì brom có dư, nên ptpư: C2H2 + 2Br2 → C2H2Br4
0,02 0,04
mBr = 160 . 0,04 = 6,4 (g)
Bài 23. Hỗn hợp A gồm C2H2, H2 có tỉ khối đối với hiđro là 5. Hãy xác dnh:
a) %V mỗi khí trong hỗn hợp A.
b) Nếu đốt cháy hoàn toàn 6,72 lít hỗn hợp A (đktc) sản phẩm cháy được dẫn vào bình chứa dung dịch Ca(OH)3 dư. Hỏi khối lượng bình tăng bao nhiêu gam. Tính khối lượng kết tủa tạo thành.
Hướng dẫn giải:
a) Khối lượng của 1 mol hỗn hợp A: M = 5.2 = 10
Đặt: 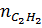 = x →
= x → 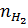 = 1- x, ta có:
M = 26x + 2(1 - x) = 10
x =
= 1- x, ta có:
M = 26x + 2(1 - x) = 10
x =  g mol C2H2 và 1 -
g mol C2H2 và 1 -  =
=  mol H2
%C2H2 = 33,33%; %H2 = 66,67%.
b) nA =
mol H2
%C2H2 = 33,33%; %H2 = 66,67%.
b) nA = 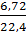 = 0,3 → 0,1 mol C2H2 và 0,2 mol H2
C2H2 + 2,5O2 → 2CO2↑ + H2O
0,1 0,2 0,1 mol
H2 + 0,5O2 → H2O
0,2 0,2 mol
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,2 0,2 mol
= 0,3 → 0,1 mol C2H2 và 0,2 mol H2
C2H2 + 2,5O2 → 2CO2↑ + H2O
0,1 0,2 0,1 mol
H2 + 0,5O2 → H2O
0,2 0,2 mol
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,2 0,2 mol
 mB =
mB = 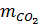 +
+ 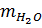 = 44.0,2 + 18(0,1 + 0,2) = 14,2 (gam)
= 44.0,2 + 18(0,1 + 0,2) = 14,2 (gam)
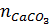 =
= 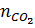 = 0,2 ⇒
= 0,2 ⇒ 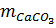 = 100 x 0,2 = 20(g)
Bài 24. Dẫn 1,12 lít (đktc) hỗn hợp A gồm C2H4, C2H2 vào bình chứa dung dịch Br2. Thấy nước brom nhạt màu một phần và khối lượng của bình tăng lên 1,34(g). Tính % thể tích mỗi khí trong A.
Hướng dẫn giải:
C2H4 + Br2 → C2H4Br2
x
C2H2 + 2Br2 → C2H2Br4
y
nA =
= 100 x 0,2 = 20(g)
Bài 24. Dẫn 1,12 lít (đktc) hỗn hợp A gồm C2H4, C2H2 vào bình chứa dung dịch Br2. Thấy nước brom nhạt màu một phần và khối lượng của bình tăng lên 1,34(g). Tính % thể tích mỗi khí trong A.
Hướng dẫn giải:
C2H4 + Br2 → C2H4Br2
x
C2H2 + 2Br2 → C2H2Br4
y
nA = 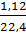 = 0,05 (mol)
mA =
= 0,05 (mol)
mA =  mbình = 1,34 (g)
Gọi x, y là số mol C2H4 và C2H2 trong hỗn hợp ta có:
nA = x + y = 0,05 (1)
mA = 28x + 26y = 1,34 (2)
Giải hệ (1), (2) ta được:
x = 0,02 mol C2H4 → % C2H4 =
mbình = 1,34 (g)
Gọi x, y là số mol C2H4 và C2H2 trong hỗn hợp ta có:
nA = x + y = 0,05 (1)
mA = 28x + 26y = 1,34 (2)
Giải hệ (1), (2) ta được:
x = 0,02 mol C2H4 → % C2H4 = 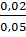 x 100 = 40%
y = 0,03 mol C2H2 → % C2H2 =
x 100 = 40%
y = 0,03 mol C2H2 → % C2H2 = 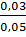 x 100 = 60%
Bài 25. Cho 10 gam hỗn hợp A gồm CaC2, CaO tác dụng với nước dư, thu được 2,24 lít một chất khí (đktc).
a) Viết các phương trình phản ứng xảy ra.
b) Tính % khối lượng mỗi chất trong A.
Hướng dẫn giải:
a) Phương trình phản ứng:
CaC2 + 2H2O → C2H2↑ + Ca(OH)2
CaO + H2O → Ca(OH)2
b)
x 100 = 60%
Bài 25. Cho 10 gam hỗn hợp A gồm CaC2, CaO tác dụng với nước dư, thu được 2,24 lít một chất khí (đktc).
a) Viết các phương trình phản ứng xảy ra.
b) Tính % khối lượng mỗi chất trong A.
Hướng dẫn giải:
a) Phương trình phản ứng:
CaC2 + 2H2O → C2H2↑ + Ca(OH)2
CaO + H2O → Ca(OH)2
b) 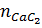 =
= 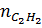 =
= 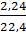 = 0,1 (mol)
= 0,1 (mol)
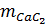 = 64 x 0,1 = 6,4
%CaC2 =
= 64 x 0,1 = 6,4
%CaC2 = 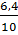 x 100 = 64%
%CaO = (100 - 64)% = 36%
Bài 26. X là một hiđrocacbon có tỉ lệ số nguyên tử của các nguyên tố là: 1:1. Mặt khác khi đốt cháy hoàn toàn 1 mol X thì thu được số mol CO2 nằm trong khoảng 5 <
x 100 = 64%
%CaO = (100 - 64)% = 36%
Bài 26. X là một hiđrocacbon có tỉ lệ số nguyên tử của các nguyên tố là: 1:1. Mặt khác khi đốt cháy hoàn toàn 1 mol X thì thu được số mol CO2 nằm trong khoảng 5 < 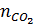 < 7.
a) Xác định công thức phân tử của X.
b) Biết X có cấu tạo mạch vòng, liên kết đơn xen kẽ với liên kết đôi. Xác định công thức cấu tạo của X, đọc tên.
Hướng dẫn giải:
a) X có dạng CnHn, phương trình phản ứng cháy:
CnHn +
< 7.
a) Xác định công thức phân tử của X.
b) Biết X có cấu tạo mạch vòng, liên kết đơn xen kẽ với liên kết đôi. Xác định công thức cấu tạo của X, đọc tên.
Hướng dẫn giải:
a) X có dạng CnHn, phương trình phản ứng cháy:
CnHn + 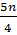 O2 → nCO2 +
O2 → nCO2 +  H2O
1 n (mol)
Theo giả thiết: 5 < n < 7
b) Vì n nguyên → n = 6. Vậy CTPT của X là: C6H6
(Benzen)
Bài 27. Y là một hiđrocacbon, trong những điều kiện thích hợp, Y tác dụng được với brom khan tạo thành sản phẩm chứa 1 nguyên tử brom, trong đó brom chiếm 50,95% khối lượng. Xác định CTPT của Y viết phương trình phản ứng xảy ra.
Hướng dẫn giải:
Sản phẩm chứa brom có dạng CxHyBr. Theo giả thiết ta có:
My = 12x + y + 80 = 80.
H2O
1 n (mol)
Theo giả thiết: 5 < n < 7
b) Vì n nguyên → n = 6. Vậy CTPT của X là: C6H6
(Benzen)
Bài 27. Y là một hiđrocacbon, trong những điều kiện thích hợp, Y tác dụng được với brom khan tạo thành sản phẩm chứa 1 nguyên tử brom, trong đó brom chiếm 50,95% khối lượng. Xác định CTPT của Y viết phương trình phản ứng xảy ra.
Hướng dẫn giải:
Sản phẩm chứa brom có dạng CxHyBr. Theo giả thiết ta có:
My = 12x + y + 80 = 80. 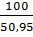 = 157
y = 77 – 12x
Kết hợp với công thức của các chất được học trong chương trình, chỉ có x = 6, y = 5 là phù hợp.
= 157
y = 77 – 12x
Kết hợp với công thức của các chất được học trong chương trình, chỉ có x = 6, y = 5 là phù hợp.
Công thức của sản phẩm: C6H5Br.
Công thức của Y là C6H6
Phương trình phản ứng:
C6H6+ Br2 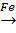 C6H6Br + HBr.
(khan)
Bài 28. Người ta điều chế benzen từ axetilen theo phương trình:
3C2H2
C6H6Br + HBr.
(khan)
Bài 28. Người ta điều chế benzen từ axetilen theo phương trình:
3C2H2 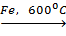 C6H6
Nếu dùng 26,88 lít axetilen (đktc) thì điều chế được bao nhiêu ml benzen. Biết hiệu suất phản ứng là 90% và khối lượng riêng của brom là 0,8 gam/ml.
Hướng dẫn giải:
C6H6
Nếu dùng 26,88 lít axetilen (đktc) thì điều chế được bao nhiêu ml benzen. Biết hiệu suất phản ứng là 90% và khối lượng riêng của brom là 0,8 gam/ml.
Hướng dẫn giải:
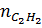 =
= 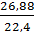 = 1,2 (mol)
Phương trình phản úmg:
3C2H2 Fe,
= 1,2 (mol)
Phương trình phản úmg:
3C2H2 Fe, 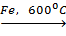 C6H6
C6H6
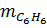 (lí thuyết) = 78 . 0,4 = 31,2 (gam)
(lí thuyết) = 78 . 0,4 = 31,2 (gam)
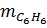 (thực tế) = 31,2 .
(thực tế) = 31,2 . 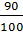 = 28,08 (gam)
= 28,08 (gam)
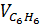 =
= 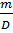 =
= 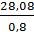 = 35,1 (ml)
Bài 29. Khí thiên nhiên có thành phần 96%CH4, 2% CO2, 2% N2 về thể tích. Hãy tính:
a) Tỉ khối của hỗn hợp trên đối với H2.
b) Thể tích không khí chứa 20% O2 để đốt cháy 2,24 lít hỗn hợp khí trên.
Hướng dẫn giải:
a) 1 mol hỗn hợp khí thiên nhiên có khối lượng:
= 35,1 (ml)
Bài 29. Khí thiên nhiên có thành phần 96%CH4, 2% CO2, 2% N2 về thể tích. Hãy tính:
a) Tỉ khối của hỗn hợp trên đối với H2.
b) Thể tích không khí chứa 20% O2 để đốt cháy 2,24 lít hỗn hợp khí trên.
Hướng dẫn giải:
a) 1 mol hỗn hợp khí thiên nhiên có khối lượng:
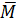 =
= 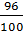 .16 +
.16 + 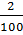 . 28 +
. 28 + 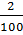 .44 = 16,8 (g)
.44 = 16,8 (g)
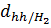 =
= 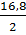 = 8,4
b)
= 8,4
b) 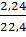 = 0,1 mol khí có
= 0,1 mol khí có 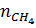 = 0,1 x
= 0,1 x 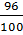 = 0,096
Chỉ có CH4 cháy được theo phương trình:
CH4 + 2O2 → CO2 + 2H2O
0,096 ..2.0,096 = 0,192 (mol)
= 0,096
Chỉ có CH4 cháy được theo phương trình:
CH4 + 2O2 → CO2 + 2H2O
0,096 ..2.0,096 = 0,192 (mol)
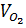 = 22,4 x 0,192 = 4,3008 tlít)
V(không khí) = 4,3008 .
= 22,4 x 0,192 = 4,3008 tlít)
V(không khí) = 4,3008 . 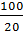 = 21,504 (lít)
= 21,504 (lít)
© Bản quyền thuộc về
Bài kiểm tra. Ghi rõ nguồn Bài kiểm tra.com khi sao chép nội dung này.