Giải bài tập Hóa học 8, Bài 33: Điều chế hiđro – phản ứng thế
2019-07-12T00:09:09-04:00
2019-07-12T00:09:09-04:00
Giải bài tập Hóa học 8, Bài 33: Điều chế hiđro – phản ứng thế : Hướng dẫn trả lời câu hỏi và bài tập.
/themes/cafe/images/no_image.gif
Bài Kiểm Tra
https://baikiemtra.com/uploads/bai-kiem-tra-logo.png
Thứ sáu - 12/07/2019 00:08
Giải bài tập Hóa học 8, Bài 33: Điều chế hiđro – phản ứng thế : Hướng dẫn trả lời câu hỏi và bài tập.
1. Những phản ứng hoá học nào dưới đây có thể được dùng để điều chế hiđro trong phòng thí nghiệm?
3) Zn + H2SO4 → ZnSO4 + H2↑
b) 2H2O 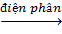 2H2↑ + O2↑
c) 2Al + 6HCl → 2AlCl3 + 3H2↑
HƯỚNG DẪN GIẢI:
Phản ứng hoá học điều chế H2 trong phòng thí nghiệm: a) và c).
2. Lập phương trình hoá học của các phản ứng sau đây và cho biết chúng thuộc loại phản ứng hoá học nào?
a) Mg + O2 -----> MgO
b) KMnO4 ------> K2MnO4 + MnO2 + O2
c) Fe + CuCl2 -----> FeCl2 + Cu
HƯỚNG DẪN GIẢI:
Phản ứng a) là phản ứng hoá hợp, phản ứng b) là phản ứng oxi hoá - khử (phản ứng phân hủy), phản ứng c) là phản ứng thế.
3. Khi thu khí oxi vào ống nghiệm bằng cách đẩy không khí, phải để vị trí ống nghiệm như thế nào? Vì sao? Đối với khí hiđro, có làm thế được không? Vì sao?
HƯỚNG DẪN GIẢI:
Vì khí O2 (M = 32) nặng hơn không khí (M = 29) nên khi thu khí oxi ta có thể để ống nghiệm nghiêng hoặc để đứng, còn khí H2 nhẹ hơn không khí nên khi thu khí H2 phải úp ngược ống nghiệm, không được để đứng ống nghiệm.
4. Trong phòng thí nghiệm có các kim loại kẽm và sắt, dung dịch axit clohiđric HCl và axit sunturic H2SO4 loãng:
a) Viết các phương trình hoá học có thể điều chế hiđro;
b) Phải dùng bao nhiêu gam kẽm, bao nhiêu gam sắt để điều chế được 2,24 lít khí hiđro (ở đktc)?
a) Phương trình hoá học của các phản ứng:
Fe + H2SO4 loãng → FeSO4 + H2↑ (1)
Zn + H2SO4 → ZnSO4 + H2↑ (2)
Fe + 2HCl → FeCl2 + H2↑ (3)
Zn + 2HCl → ZnCl2 + H2↑ (4)
b) nH =
2H2↑ + O2↑
c) 2Al + 6HCl → 2AlCl3 + 3H2↑
HƯỚNG DẪN GIẢI:
Phản ứng hoá học điều chế H2 trong phòng thí nghiệm: a) và c).
2. Lập phương trình hoá học của các phản ứng sau đây và cho biết chúng thuộc loại phản ứng hoá học nào?
a) Mg + O2 -----> MgO
b) KMnO4 ------> K2MnO4 + MnO2 + O2
c) Fe + CuCl2 -----> FeCl2 + Cu
HƯỚNG DẪN GIẢI:
Phản ứng a) là phản ứng hoá hợp, phản ứng b) là phản ứng oxi hoá - khử (phản ứng phân hủy), phản ứng c) là phản ứng thế.
3. Khi thu khí oxi vào ống nghiệm bằng cách đẩy không khí, phải để vị trí ống nghiệm như thế nào? Vì sao? Đối với khí hiđro, có làm thế được không? Vì sao?
HƯỚNG DẪN GIẢI:
Vì khí O2 (M = 32) nặng hơn không khí (M = 29) nên khi thu khí oxi ta có thể để ống nghiệm nghiêng hoặc để đứng, còn khí H2 nhẹ hơn không khí nên khi thu khí H2 phải úp ngược ống nghiệm, không được để đứng ống nghiệm.
4. Trong phòng thí nghiệm có các kim loại kẽm và sắt, dung dịch axit clohiđric HCl và axit sunturic H2SO4 loãng:
a) Viết các phương trình hoá học có thể điều chế hiđro;
b) Phải dùng bao nhiêu gam kẽm, bao nhiêu gam sắt để điều chế được 2,24 lít khí hiđro (ở đktc)?
a) Phương trình hoá học của các phản ứng:
Fe + H2SO4 loãng → FeSO4 + H2↑ (1)
Zn + H2SO4 → ZnSO4 + H2↑ (2)
Fe + 2HCl → FeCl2 + H2↑ (3)
Zn + 2HCl → ZnCl2 + H2↑ (4)
b) nH = 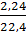 = 0,1 mol
Theo phương trình:
= 0,1 mol
Theo phương trình:
(3) mFe cần dùng: 56 x 0,1 = 5,6g
(4) mZn cần dùng: 65 x 0,1 = 6,5g.
5. Cho 22,4g sắt tác dụng với dung dịch loãng có chứa 24,5g axit sunturic.
a) Chất nào còn dư sau phản ứng và dư bao nhiêu gam?
b) Tính thể tích khí hiđro thu được ở đktc.
HƯỚNG DẪN GIẢI:
nFe = 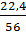 = 0,4mol;
= 0,4mol;
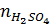 =
= 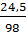 = 0,25 mol
a) Phương trình hoá học của phản ứng
Fe + H2SO4 → FeSO4 + H2↑
1 mol 1 mol
So sánh tỉ lệ:
= 0,25 mol
a) Phương trình hoá học của phản ứng
Fe + H2SO4 → FeSO4 + H2↑
1 mol 1 mol
So sánh tỉ lệ: 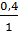 >
> 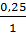 →khối lượng Fe dư.
mFe dư: (0,4 - 0,25) x 56 = 8,4g
b) Theo phương trình phản ứng trên:
Do khối lượng Fe dư nên tính thể tích khí H2 theo số mol H2SO4
→khối lượng Fe dư.
mFe dư: (0,4 - 0,25) x 56 = 8,4g
b) Theo phương trình phản ứng trên:
Do khối lượng Fe dư nên tính thể tích khí H2 theo số mol H2SO4
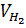 = 0,25 x 22,4 = 5,6 lít.
= 0,25 x 22,4 = 5,6 lít.
© Bản quyền thuộc về
Bài kiểm tra. Ghi rõ nguồn Bài kiểm tra.com khi sao chép nội dung này.