Giải bài tập Hóa học 9, Bài 20: Hợp kim sắt: gang, thép.
2019-06-30T22:39:09-04:00
2019-06-30T22:39:09-04:00
Giải bài tập Hóa học 9, Bài 20: Hợp kim sắt: gang, thép.
/themes/cafe/images/no_image.gif
Bài Kiểm Tra
https://baikiemtra.com/uploads/bai-kiem-tra-logo.png
Chủ nhật - 30/06/2019 22:39
Giải bài tập Hóa học 9, Bài 20: Hợp kim sắt: gang, thép.
Bài 1. Thế nào là hợp kim? Thế nào là gang và thép? Nêu thành phần, tính chất, ứng dụng của gang và thép.
Hướng dẫn giải: Xem sách giáo khoa Hóa học 9.
Bài 2. Hãy cho biết nguyên tắc sản xuất gang và viết các phương trình hóa học.
Hướng dẫn giải:
Nguyên tắc sản xuất gang là dùng cacbon monoxit khử oxit sắt ở nhiệt độ cao trong lò luyện kim (lò cao).
Các phương trình hóa học:
C(r) + O2(k) → CO2(k) (1)
C(r) + CO2(k) → 2CO (k) (2)
3CO(k) + Fe2O3(r) → 2Fe + 3CO2(k) (3)
Bài 3. Hãy cho biết nguyên tắc luyện gang thành thép và viết các phương trình hóa học.
Hướng dẫn giải:
Nguyên tắc luyện gang thành thép: oxi hóa một số kim loại, phi kim để đưa ra khỏi gang phần lớn các nguyên tố cacbon, silic, mangan...
Các phương trình hóa học.
2Fe + O2 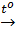 2FeO (1)
FeO + C
2FeO (1)
FeO + C 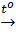 Fe + CO↑ (2)
2FeO + Si
Fe + CO↑ (2)
2FeO + Si 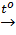 2Fe + SiO2 (3)
FeO + Mn
2Fe + SiO2 (3)
FeO + Mn 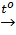 Fe + MnO (4)
Bài 4. Những khí thải (CO2, SO2...) trong quá trình sản xuất gang thép có ảnh huởng như thế nào đến môi trường xung quanh? Dẫn ra một số phản ứng để giải thích. Thử nêu biện pháp để chống ô nhiễm môi trường ở khu dân cư gần cơ sở sản xuất gang thép.
Hướng dẫn giải:
CO2 là nguyên nhân chính gây ra hiệu ứng nhà kính làm cho Trái đất ấm dần, băng hai cực tan nhanh có thể nhấn chìm nhiều thành phố, làng mạc ven biển.
SO2 là nguyên nhân gây ra hiện tượng mưa axit, pH thấp làm cho động thực vật bị chết, phá hủy các công trình xây dựng ...
2SO2 + O2 → 2SO3
5O2 + H2O → H2SO3
5O3 + H2O → H2SO4
Để chống ô nhiễm các khí trên có thể dùng các biện pháp sau:
- Trồng nhiều cây xanh trong khu vực dân cư cạnh nhà máy để làm giảm khí CO2.
- Xây dựng hệ thống xử lí khí thải, thu hồi SO2.
Bài 5. Hãy lập các phương trình phản ứng theo sơ đồ sau đây:
a) FeO + Mn
Fe + MnO (4)
Bài 4. Những khí thải (CO2, SO2...) trong quá trình sản xuất gang thép có ảnh huởng như thế nào đến môi trường xung quanh? Dẫn ra một số phản ứng để giải thích. Thử nêu biện pháp để chống ô nhiễm môi trường ở khu dân cư gần cơ sở sản xuất gang thép.
Hướng dẫn giải:
CO2 là nguyên nhân chính gây ra hiệu ứng nhà kính làm cho Trái đất ấm dần, băng hai cực tan nhanh có thể nhấn chìm nhiều thành phố, làng mạc ven biển.
SO2 là nguyên nhân gây ra hiện tượng mưa axit, pH thấp làm cho động thực vật bị chết, phá hủy các công trình xây dựng ...
2SO2 + O2 → 2SO3
5O2 + H2O → H2SO3
5O3 + H2O → H2SO4
Để chống ô nhiễm các khí trên có thể dùng các biện pháp sau:
- Trồng nhiều cây xanh trong khu vực dân cư cạnh nhà máy để làm giảm khí CO2.
- Xây dựng hệ thống xử lí khí thải, thu hồi SO2.
Bài 5. Hãy lập các phương trình phản ứng theo sơ đồ sau đây:
a) FeO + Mn 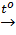 Fe + MnO
b) Fe2O3 + CO
Fe + MnO
b) Fe2O3 + CO 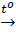 Fe + CO2↑
c) FeO + Si
Fe + CO2↑
c) FeO + Si 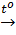 Fe + SiO2
d) FeO + C
Fe + SiO2
d) FeO + C 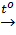 Fe + CO
Cho biết phản ứng nào xảy ra trong quá trình luyện gang, phản ứng nào xảy ra trong quá trình luyện thép, chất nào là chất oxi hóa, chất nào là chất khử?
Hướng dẫn giải:
FeO + Mn
Fe + CO
Cho biết phản ứng nào xảy ra trong quá trình luyện gang, phản ứng nào xảy ra trong quá trình luyện thép, chất nào là chất oxi hóa, chất nào là chất khử?
Hướng dẫn giải:
FeO + Mn 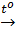 Fe + MnO (a)
Fe2O3 + 3CO
Fe + MnO (a)
Fe2O3 + 3CO 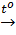 2Fe + 3CO2 (b)
2FeO + Si
2Fe + 3CO2 (b)
2FeO + Si 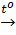 2Fe + SiO2 (c)
FeO + C
2Fe + SiO2 (c)
FeO + C 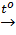 Fe + CO↑ (d)
Các phản ứng xảy ra trong quá trình luyện gang: b Các phản ứng xảy ra trong quá trình luyện thép: a, c, d.
Bài 6. Tính khối lượng quặng hematit chứa 90% Fe2O3 cần thiết để sản xuất được 1 tấn gang chứa 95% Fe. Biết hiệu suất của quá trình là 80%.
Hướng dẫn giải:
Fe2O3 + 3CO → 2Fe + 3CO2↑
1mol 2mol
160 112
x tấn 0,95 tấn
x =
Fe + CO↑ (d)
Các phản ứng xảy ra trong quá trình luyện gang: b Các phản ứng xảy ra trong quá trình luyện thép: a, c, d.
Bài 6. Tính khối lượng quặng hematit chứa 90% Fe2O3 cần thiết để sản xuất được 1 tấn gang chứa 95% Fe. Biết hiệu suất của quá trình là 80%.
Hướng dẫn giải:
Fe2O3 + 3CO → 2Fe + 3CO2↑
1mol 2mol
160 112
x tấn 0,95 tấn
x = 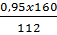 Mặt khác hiệu suất là 0,8 và quặng hematit chỉ có 90% Fe2O3 do đó khối lượng quặng hematit cần sử dụng là:
Mặt khác hiệu suất là 0,8 và quặng hematit chỉ có 90% Fe2O3 do đó khối lượng quặng hematit cần sử dụng là:
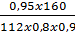 = 1,885 (tấn)
= 1,885 (tấn)
© Bản quyền thuộc về
Bài kiểm tra. Ghi rõ nguồn Bài kiểm tra.com khi sao chép nội dung này.