Giải bài tập Hóa học 9, Bài 25: Tính chất của phi kim.
2019-07-02T00:14:31-04:00
2019-07-02T00:14:31-04:00
Giải bài tập Hóa học 9, Bài 25: Tính chất của phi kim.
/themes/cafe/images/no_image.gif
Bài Kiểm Tra
https://baikiemtra.com/uploads/bai-kiem-tra-logo.png
Thứ ba - 02/07/2019 00:14
Giải bài tập Hóa học 9, Bài 25: Tính chất của phi kim.
Bài 1. Hãy chọn câu đúng:
a) phi kim dẫn điện tốt.
b) Phi kim dẫn nhiệt tốt.
c) Phi kim chỉ tồn tại ở hai trạng thái rắn, khí.
d) Phi kim dẫn điện, dẫn nhiệt kém.
Hướng dẫn giải: Phương án đúng là d.
Bài 2. Viết các phương trình hóa học của S, C, Cu, Zn với khí O2. Cho biết các oxit tạo thành thuộc loại nào. Viết công thức các axit hoặc bazơ tương ứng với mỗi oxit đó.
Hướng dẫn giải:
| Phương trình hóa học |
Axit tương ứng |
Bazơ tương ứng |
| S + O2 → SO2 oxit axit |
H2SO3 |
|
| C + O2 → CO2 oxit axit |
H2CO3 |
|
| 2Cu + O2 → 2CuO oxit bazơ |
|
Cu(OH)2 |
| 2Zn+ O2 → 2ZnO oxit lưỡng tính |
H2ZnO2 |
Zn(OH)2 |
Bài 3. Viết các phương trình hóa học và ghi đầy đủ điều kiện khi cho hiđro phản ứng với: a) Clo b) Lưu huỳnh c) Brom
Cho biết trạng thái của các chất tạo thành.
Hướng dẫn giải:
a) H2 + Cl2 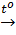 2HCl (khí)
b) H2 + S
2HCl (khí)
b) H2 + S 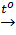 H2S (khí)
c) H2 + Br2
H2S (khí)
c) H2 + Br2 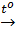 2HBr (khí)
Bài 4. Viết các phương trình hóa học giữa các cặp chất sau đây (ghi rõ điều kiện, nếu có):
a) Khí flo và hiđro; b) Bột sắt và bột lưu huỳnh;
c) Cacbon và oxi; d) Khí hiđro và lưu huỳnh.
Hướng dẫn giải:
a) Khí flo và hiđro:
H2 + F2 → 2HF (khí)
b) Bột sắt và bột lưu huỳnh: Fe + S → FeS
c) Cacbon và oxi: C + O2 → CO2
d) Khí hiđro và lưu huỳnh: H2 + S → H2S
Bài 5. Cho sơ đồ biểu diễn chuyển hóa aau:
Phi kim oxit axit
2HBr (khí)
Bài 4. Viết các phương trình hóa học giữa các cặp chất sau đây (ghi rõ điều kiện, nếu có):
a) Khí flo và hiđro; b) Bột sắt và bột lưu huỳnh;
c) Cacbon và oxi; d) Khí hiđro và lưu huỳnh.
Hướng dẫn giải:
a) Khí flo và hiđro:
H2 + F2 → 2HF (khí)
b) Bột sắt và bột lưu huỳnh: Fe + S → FeS
c) Cacbon và oxi: C + O2 → CO2
d) Khí hiđro và lưu huỳnh: H2 + S → H2S
Bài 5. Cho sơ đồ biểu diễn chuyển hóa aau:
Phi kim oxit axit 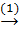 oxit axit
oxit axit  axit
axit  muối sunfat tan
muối sunfat tan  muối sunfat không tan
a) Tìm công thức các chất thích hợp để thay cho tên chất trong sơ đồ.
b) Viết các phương trình hóa học biểu diễn chuyển hóa trên.
Hướng dẫn giải:
a) S
muối sunfat không tan
a) Tìm công thức các chất thích hợp để thay cho tên chất trong sơ đồ.
b) Viết các phương trình hóa học biểu diễn chuyển hóa trên.
Hướng dẫn giải:
a) S  SO2
SO2  SO3
SO3  H2SO4
H2SO4  Na2SO4
Na2SO4  BaSO4
b) Viết các phương trình hóa học biểu diễn chuyển hóa trên.
S + O2 → SO2 (1)
2SO2 + O2
BaSO4
b) Viết các phương trình hóa học biểu diễn chuyển hóa trên.
S + O2 → SO2 (1)
2SO2 + O2 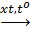 2SO3 (2)
SO3 + H2O → H2SO4 (3)
H2SO4+ 2NaOH → Na2SO4 + 2H2O (4)
Na2SO4 + BaCl2 → BaSO4↓ + 2NaCl (5)
Bài 6. Đốt hỗn hợp gồm 6,6gam sắt và 1,6 gam lưu huỳnh trong nôi trường không có không khí thu được hỗn hợp chất rắn A. Cho dung dịth HCl 1M phản ứng vừa đủ với A thu được hỗn hợp khí B.
a) Hãy viết các phương trình hóa học.
b) Tính thể tích dung dịch HCl 1M đã tham gia phản ứng.
Hướng dẫn giải:
a) Các phương trình hóa học:
Fe + S → FeS (1)
nFe =
2SO3 (2)
SO3 + H2O → H2SO4 (3)
H2SO4+ 2NaOH → Na2SO4 + 2H2O (4)
Na2SO4 + BaCl2 → BaSO4↓ + 2NaCl (5)
Bài 6. Đốt hỗn hợp gồm 6,6gam sắt và 1,6 gam lưu huỳnh trong nôi trường không có không khí thu được hỗn hợp chất rắn A. Cho dung dịth HCl 1M phản ứng vừa đủ với A thu được hỗn hợp khí B.
a) Hãy viết các phương trình hóa học.
b) Tính thể tích dung dịch HCl 1M đã tham gia phản ứng.
Hướng dẫn giải:
a) Các phương trình hóa học:
Fe + S → FeS (1)
nFe = 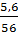 = 0,1 mol; nS =
= 0,1 mol; nS = 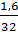 = 0,05 mol ⇒ Fe còn dư.
Hỗn hợp A gồm Fe dư 0,05mol và FeS 0,05mol.
Fe + 2HCl → FeCl2 + H2↑ (2)
FeS + 2HCl → FeCl2 + H2S↑ (3)
Hỗn hợp B gồm H2 dư và H2S.
b) Tính thể tích dung dịch HCl 1M đã tham gia phản ứng
Theo phương trình hóa học (2) và (3) tổng số mol HCl bằng hai lần tổng số mol Fe và FeS = (0,05 + 0,05) x 2 = 0,2 (mol)
Thể tích dung dịch HCl 1M =
= 0,05 mol ⇒ Fe còn dư.
Hỗn hợp A gồm Fe dư 0,05mol và FeS 0,05mol.
Fe + 2HCl → FeCl2 + H2↑ (2)
FeS + 2HCl → FeCl2 + H2S↑ (3)
Hỗn hợp B gồm H2 dư và H2S.
b) Tính thể tích dung dịch HCl 1M đã tham gia phản ứng
Theo phương trình hóa học (2) và (3) tổng số mol HCl bằng hai lần tổng số mol Fe và FeS = (0,05 + 0,05) x 2 = 0,2 (mol)
Thể tích dung dịch HCl 1M = 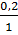 = 0,2(lit)
= 0,2(lit)
© Bản quyền thuộc về
Bài kiểm tra. Ghi rõ nguồn Bài kiểm tra.com khi sao chép nội dung này.