Giải bài tập Hóa học 9, Bài 26: Clo
2019-07-02T03:35:11-04:00
2019-07-02T03:35:11-04:00
Giải bài tập Hóa học 9, Bài 26: Clo
/themes/cafe/images/no_image.gif
Bài Kiểm Tra
https://baikiemtra.com/uploads/bai-kiem-tra-logo.png
Thứ ba - 02/07/2019 03:35
Giải bài tập Hóa học 9, Bài 26: Clo
Bài 1. Khi dẫn khí clo vào nước xảy ra hiện tượng vật lí hay hiện tượng hóa học? Hãy giải thích.
Hướng dẫn giải:
Khi dẫn khí clo vào nước xảy ra cả hiện tượng vật lí và hiện tượng hóa học. Giải thích: Clo tan trong nước là hiện tượng vật lí.
Clo còn phản ứng với nước:
Cl2 + H2O → HCl + HClO
Bài 2. Nêu tính chất hóa học của clo. Viết các phương trình hóa học minh họa.
Hướng dẫn giải: Xem sách giáo khoa Hóa học 9.
Bài 3. Viết phương trình hóa học khi cho clo, lưu huỳnh, oxi phản ứng với sắt ở nhiệt độ cao. Cho biết hóa trị của sắt trong những hợp chất tạo thành.
Hướng dẫn giải:
2Fe + 3Cl2 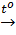 2FeCl3 ; Fe có hóa trị III
Fe + S
2FeCl3 ; Fe có hóa trị III
Fe + S 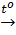 FeS; Fe có hóa trị II.
3Fe + 2O2
FeS; Fe có hóa trị II.
3Fe + 2O2 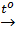 Fe3O4; Fe có hóa trị II và III.
Bài 4. Sau khi làm thí nghiệm, khí clo dư được loại bỏ bằng cách sục khí clo vào:
a) Dung dịch HCl; b) Dung dịch NaOH
c) Dung dịch NaCl; d) Nước.
Trường hợp nào đúng? Hãy giải thích.
Hướng dẫn giải: Trường hợp b đúng, bởi vì xảy ra phản ứng hóa học:
Cl2 + 2NaOH → NaCl + NaClO + H2O
Bài 5. Dẫn khí clo vào dung dịch KOH, tạo thành dung dịch hai muối. Hãy viết các phương trình hóa học.
Hướng dẫn giải:
Cl2 + 2KOH → KCl + KClO + H2O
Bài 6. Có ba khí được đựng riêng biệt trong ba lọ là: clo, hiđro clorua, oxi. Hãy nêu phương pháp hóa học để nhận biết từng khí dựng trong mỗi lọ.
Hướng dẫn giải:
Dùng tàn đóm đỏ để nhận ra khí oxi, tàn đóm sẽ bùng cháy thành ngọn lửa trong khí oxi. Hai lọ còn lại dùng giấy quỳ tím tẩm ướt để phân biệt, nếu quỳ chuyển sang màu đỏ thì đó là lọ đựng khí HCl, nếu quỳ tim mất màu thì đó là 1 khí clo.
Bài 7. Nêu phương pháp điều chế khí clo trong phòng thí nghiệm. Viết phương trình hóa học minh họa.
Hướng dẫn giải:
Có thể sử đụng các chất oxi hóa như MnO2, KMnO4 tác dụng với dunj dịch axit HCl đặc.
MnO2 + 4HCl → MnCl2 + Cl2↑ + 2H2O
2KMnO4 + 16HCl → 2KC1 + 2MnCl2 + 5Cl2↑ + 8H2O
Bài 8. Trong công nghiệp, clo được điều chế bằng phương pháp nào? Viết phương trình phản ứng.
Hướng dẫn giải:
Trong công nghiệp, clo được điều chế ở quy mô lớn, giá thành rẻ bằng cách điện phân dung dịch muối ăn bão hoà có màng ngăn.
2NaCl + 2H2O
Fe3O4; Fe có hóa trị II và III.
Bài 4. Sau khi làm thí nghiệm, khí clo dư được loại bỏ bằng cách sục khí clo vào:
a) Dung dịch HCl; b) Dung dịch NaOH
c) Dung dịch NaCl; d) Nước.
Trường hợp nào đúng? Hãy giải thích.
Hướng dẫn giải: Trường hợp b đúng, bởi vì xảy ra phản ứng hóa học:
Cl2 + 2NaOH → NaCl + NaClO + H2O
Bài 5. Dẫn khí clo vào dung dịch KOH, tạo thành dung dịch hai muối. Hãy viết các phương trình hóa học.
Hướng dẫn giải:
Cl2 + 2KOH → KCl + KClO + H2O
Bài 6. Có ba khí được đựng riêng biệt trong ba lọ là: clo, hiđro clorua, oxi. Hãy nêu phương pháp hóa học để nhận biết từng khí dựng trong mỗi lọ.
Hướng dẫn giải:
Dùng tàn đóm đỏ để nhận ra khí oxi, tàn đóm sẽ bùng cháy thành ngọn lửa trong khí oxi. Hai lọ còn lại dùng giấy quỳ tím tẩm ướt để phân biệt, nếu quỳ chuyển sang màu đỏ thì đó là lọ đựng khí HCl, nếu quỳ tim mất màu thì đó là 1 khí clo.
Bài 7. Nêu phương pháp điều chế khí clo trong phòng thí nghiệm. Viết phương trình hóa học minh họa.
Hướng dẫn giải:
Có thể sử đụng các chất oxi hóa như MnO2, KMnO4 tác dụng với dunj dịch axit HCl đặc.
MnO2 + 4HCl → MnCl2 + Cl2↑ + 2H2O
2KMnO4 + 16HCl → 2KC1 + 2MnCl2 + 5Cl2↑ + 8H2O
Bài 8. Trong công nghiệp, clo được điều chế bằng phương pháp nào? Viết phương trình phản ứng.
Hướng dẫn giải:
Trong công nghiệp, clo được điều chế ở quy mô lớn, giá thành rẻ bằng cách điện phân dung dịch muối ăn bão hoà có màng ngăn.
2NaCl + 2H2O 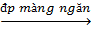 2NaOH + H2↑ + Cl2
Bài 9. Có thể thu khí clo bằng cách đẩy nước dược không? Hãy giải thích.
Có thể thu khí clo bằng cách đẩy không khí được không? Hãy giải thích và mô tả bằng hình vẽ. Cho biết vai trò của H2SO4 đặc.
Hướng dẫn giải:
- Không thể thu khí clo bằng cách đẩy nước vì clo phản ứng với nước và tan đáng kể trong nước.
- Có thể thu khí clo bằng cách đẩy không khí, có thể dùng dụng cụ theo sơ đồ sau:
Theo thứ tự từ trái qua phải là bình rửa khí đựng H2SO4 đặc để hút ẩm làm khô khí clo, bình thứ hai dựng khí clo khô, bình thứ ba đựng dung dịch NaOH để phòng clo đã đầy tràn ra không khí làm ô nhiễm.
Bài 10. Tính thể tích dung dịch NaOH 1M để tác dụng hoàn toàn với 1,12 lít khí clo (đktc). Nồng độ mol của các chất sau phản ứng là bao nhiêu. Giả thiết thể tích dung dịch thay đổi không đáng kể.
Hướng dẫn giải:
2NaOH + Cl2 → NaCl + NaClO + H2O
2NaOH + H2↑ + Cl2
Bài 9. Có thể thu khí clo bằng cách đẩy nước dược không? Hãy giải thích.
Có thể thu khí clo bằng cách đẩy không khí được không? Hãy giải thích và mô tả bằng hình vẽ. Cho biết vai trò của H2SO4 đặc.
Hướng dẫn giải:
- Không thể thu khí clo bằng cách đẩy nước vì clo phản ứng với nước và tan đáng kể trong nước.
- Có thể thu khí clo bằng cách đẩy không khí, có thể dùng dụng cụ theo sơ đồ sau:
Theo thứ tự từ trái qua phải là bình rửa khí đựng H2SO4 đặc để hút ẩm làm khô khí clo, bình thứ hai dựng khí clo khô, bình thứ ba đựng dung dịch NaOH để phòng clo đã đầy tràn ra không khí làm ô nhiễm.
Bài 10. Tính thể tích dung dịch NaOH 1M để tác dụng hoàn toàn với 1,12 lít khí clo (đktc). Nồng độ mol của các chất sau phản ứng là bao nhiêu. Giả thiết thể tích dung dịch thay đổi không đáng kể.
Hướng dẫn giải:
2NaOH + Cl2 → NaCl + NaClO + H2O
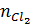 =
= 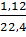 = 0,05 mol ; nNaOH = 2 x 0,05 = 0,1 mol
Tính thể tích dung dịch NaOH 1M =
= 0,05 mol ; nNaOH = 2 x 0,05 = 0,1 mol
Tính thể tích dung dịch NaOH 1M = 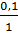 = 0,1 (lit)
Nồng độ mol của các chất sau phản ứng:
= 0,1 (lit)
Nồng độ mol của các chất sau phản ứng:
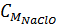 =
= 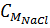 =
= 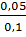 = 0,5 M
Bài 11. Cho 10,8 gam kim loại M hóa trị III tác dụng với clo dư thì thu được 53,4 gam muối. Hãy xác định kim loại M đã dùng.
Hướng dẫn giải:
Trong những bài xác định nguyên tố phải xác định khối lượng mol của nguyên tố đó rồi so sánh để biết đó là nguyên tố hóa học nào.
2M + 3Cl2 → 2MCl3
2mol 3mol
Số mol clo =
= 0,5 M
Bài 11. Cho 10,8 gam kim loại M hóa trị III tác dụng với clo dư thì thu được 53,4 gam muối. Hãy xác định kim loại M đã dùng.
Hướng dẫn giải:
Trong những bài xác định nguyên tố phải xác định khối lượng mol của nguyên tố đó rồi so sánh để biết đó là nguyên tố hóa học nào.
2M + 3Cl2 → 2MCl3
2mol 3mol
Số mol clo = 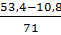 =0,6 mol
Số mol M =
=0,6 mol
Số mol M = 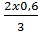 = 0,4 mol
Khối lượng mol của M =
= 0,4 mol
Khối lượng mol của M = 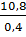 =27 ⇒ M là Al.
=27 ⇒ M là Al.
© Bản quyền thuộc về
Bài kiểm tra. Ghi rõ nguồn Bài kiểm tra.com khi sao chép nội dung này.