Giải bài tập Hóa học 8, Bài 38: Bài luyện tập 7
2019-07-13T04:05:27-04:00
2019-07-13T04:05:27-04:00
Giải bài tập Hóa học 8, Bài 38: Bài luyện tập 7 : Hướng dẫn trả lời câu hỏi và bài tập.
/themes/cafe/images/no_image.gif
Bài Kiểm Tra
https://baikiemtra.com/uploads/bai-kiem-tra-logo.png
Thứ bảy - 13/07/2019 04:05
Giải bài tập Hóa học 8, Bài 38: Bài luyện tập 7 : Hướng dẫn trả lời câu hỏi và bài tập.
1. Tương tự như natri, các kim loại kali K và canxi Ca cũng tác dụng được với nước tạo thành bazơ tan và giải phóng khí hiđro.
a) Hãy viết các phương trình phản ứng xảy ra.
b) Các phản ứng hoá học trên thuộc loại phản ứng hoá học nào?
HƯỚNG DẪN GIẢI:
a) Phương trình hoá học của phản ứng K, Ca tác dụng với nước:
2K + H2O → 2KOH + H2
Ca + 2H2O → Ca(OH)2 + H2
b) Các phản ứng trên thuộc loại phản ứng thế.
2. Hãy lập phương trình hoá học của những phản ứng có sơ đồ sau đây:
a) Na2O + H2O -----> NaOH
K2O + H2O -----> KOH
b) SO2 + H2O -----> H2SO3
SO3 + H2O -----> H2SO4
N2O5 + H2O ------> HNO3
c) NaOH + HCl ----> NaCl + H2O
Al(OH)3 + H2SO4 ----> Al2(SO4)3 + H2O
d) Chỉ ra loại chất tạo thành ở a), b) và c) là gì? Nguyên nhân có sự khác nhau ở a) và b)?
e) Gọi tên các chất tạo thành.
HƯỚNG DẪN GIẢI:
Phương trình hoá học của phản ứng:
a) Na2O + H2O → 2NaOH
K2O + H2O → 2KOH
b) SO2 + H2O → H2SO3
SO3 + H2O → H2SO4
N2O5 + H2O → 2HNO3
c) NaOH + HCl → NaCl + H2O
2Al(OH)3 + 3H2SO4 → Al2(SO4)3 + 3H2O
d) Loại chất tạo thành ở a) (NaOH, KOH) là bazơ kiềm là loại chất tan; ở b) (H2SO3, H2SO4, HNO3) là axit; ở c) (NaCl, Al2(SO4)3) là muối.
Nguyên nhân của sự khác biệt là ở a) là oxit bazơ (Na2O, K2O) tác dụng với nước cho bazơ còn ở b) là oxit axit (SO2, SO3, N2O5) tác dụng với nước cho axit.
3. Viết công thức hoá học của những muối có tên gọi dưới đây:
Đồng (II) clorua, kẽm sunfat, sắt (III) sunfat, magie hiđrocacbonat, canxi photphat, natri hiđrophotphat, natri đihiđrophotphat.
HƯỚNG DẪN GIẢI:
Công thức hoá học của những muối:
CuCl2; ZnSO4; Fe2(SO4)3; Mg(HCO3)2; Ca3(PO4)2; Na2HPO4; NaH2PO4.
4. Cho biết khối lượng mol của một oxit kim loại là 160 gam, thành phần về khối lượng của kim loại trong oxit đó là 70%. Lập công thức hoá học của oxit. Gọi tên oxit kim loại đó.
HƯỚNG DẪN GIẢI:
Đặt công thức của oxit kim loại là MxOy.
Khối lượng của kim loại trong oxit kim loại:
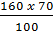 = 112g
Mx = 112, kẻ bảng ta có:
= 112g
Mx = 112, kẻ bảng ta có:
| x |
1 2 3 |
| M |
112 56 37,33
(loại) (nhận) (loại) |
Khối lượng của oxi là:
160 - 112 = 48g
16.y = 48 → y = 3
Vậy công thức hoá học của oxit kim loại là Fe2O3.
5. Nhôm (III) oxit tác dụng với axit sunturic theo phương trình phản ứng sau:
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Tính lượng muối nhôm sunfat được tạo thành nếu đã sử dụng 49g axit sunfuric nguyên chất tác dụng với 60g nhôm oxit. Sau phản ứng chất nào còn dư? Lượng dư của chất đó là bao nhiêu?
HƯỚNG DẪN GIẢI:
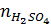 =
= 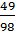 = 0,5mol;
= 0,5mol;
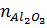 =
= 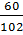
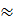 0,59 mol
Phương trình hoá học của phản ứng:
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
1 mol 3 mol
So sánh tỉ lệ:
0,59 mol
Phương trình hoá học của phản ứng:
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
1 mol 3 mol
So sánh tỉ lệ: 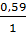 >
> 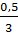 →Nhôm oxit dư, tính lượng Al2(SO4)3 theo H2SO4
- Theo phương trình phản ứng trên:
102g Al2O3 tác dụng với 294g H2SO4
→Nhôm oxit dư, tính lượng Al2(SO4)3 theo H2SO4
- Theo phương trình phản ứng trên:
102g Al2O3 tác dụng với 294g H2SO4
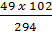 = 17 g ← 49g H2SO4
= 17 g ← 49g H2SO4
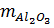 dư = 60 - 17 = 43g
- Theo phương trình phản ứng trên:
294g H2SO4 tác dụng với Al2O3 cho 342g Al2(SO4)3
Vậy 49g H2SO4 tác dụng với Al2O3 cho xg Al2(SO4)3
x =
dư = 60 - 17 = 43g
- Theo phương trình phản ứng trên:
294g H2SO4 tác dụng với Al2O3 cho 342g Al2(SO4)3
Vậy 49g H2SO4 tác dụng với Al2O3 cho xg Al2(SO4)3
x = 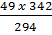 = 57g Al2(SO4)3
= 57g Al2(SO4)3
© Bản quyền thuộc về
Bài kiểm tra. Ghi rõ nguồn Bài kiểm tra.com khi sao chép nội dung này.