Tóm tắt lí thuyết Chương III - Hóa học 8
2019-07-09T05:16:27-04:00
2019-07-09T05:16:27-04:00
Tóm tắt kiến thức cần nhớ Hóa học 8, chương III, gồm các bài: Mol - Sự chuyển đổi giữa khối lượng, thể tích và lượng chất - Tỉ khối các chất khí - Tính theo công thức hóa học - Tính theo phương trình hóa học.
/themes/cafe/images/no_image.gif
Bài Kiểm Tra
https://baikiemtra.com/uploads/bai-kiem-tra-logo.png
Thứ ba - 09/07/2019 05:08
Tóm tắt kiến thức cần nhớ Hóa học 8, chương III, gồm các bài: Mol - Sự chuyển đổi giữa khối lượng, thể tích và lượng chất - Tỉ khối các chất khí - Tính theo công thức hóa học - Tính theo phương trình hóa học.
I. KIẾN THỨC CẦN NHỚ
1. Khái niệm mol
Một mol là lượng chất chứa N (6.1023) nguyên tử hoặc phân tử của chất đó.
2. Khối lượng mol (kí hiệu M)
Khối lượng mol của một chất là khối lượng của N nguyên tử hoặc phân tử chất đó, tính bằng gam, có số trị bằng nguyên tử khôi hoặc phân tử khối.
3. Thể tích mol của chất khí
- Thể tích mol của chất khí là thể tích chiếm bởi N phân tử chất đó.
- Một mol của bất kì chất khí nào, trong cùng điều kiện về nhiệt độ và áp suất đều chiếm những thể tích bằng nhau.
- Ở điều kiện tiêu chuẩn (đktc), nghĩa là nhiệt độ 0°c và áp suất 1atm (hoặc 760mmHg), 1 mol bất kì chất khí nào cũng chiếm thể tích 22,4 lít (dm3).
4. Sự liên quan giữa số mol và số hạt vi mô, khối lượng mol, khối lượng và thể tích của chất khí
a) Biến đổi giữa số mol n và số hạt vi mô (nguyên tử, phân tử...)
n = 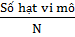 |
b) Biến đổi giữa số mol n và khối lượng m (g)
n = 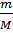 ⇒ m = n x M; M = ⇒ m = n x M; M =  |
Trong đó: m là khối lượng của một chất hay một lượng nguyên tử;
M là khối lượng mol phân tử (hay nguyên tử).
c) Biến đổi giữa số mol và thể tích của chất khí (lít)
n = 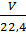 ⇒ V = n x 22,4 ⇒ V = n x 22,4 |
V: Thể tích của chất khí ở đktc.
d) Khối lượng của 1 mol phân tử khí
(D là khối lượng riêng của 1 lít khí ở đktc).
e) Công thức tính tỉ khối của khí A đối với khí B
dA/B = 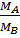 ⇒ MA = dA/B . MB ⇒ MA = dA/B . MB |
f) Công thức tính tỉ khối của khí A đối với không khí:
dA/KK = 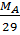 ⇒ MA = 29 .dA/KK ⇒ MA = 29 .dA/KK |
5. Thể tích của chất rắn hay chất lỏng
V = 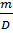 |
Trong đó D là khối lượng riêng:
D (g/cm3) có m (g) và V (cm3) hay mililít
D (kg/dm3) có m (kg) và V (dm3) hay lít.
II. HƯỚNG DẪN GIẢI BÀI TẬP TÍNH THEO CÔNG THỨC HOÁ HỌC VÀ TÍNH THEO PHƯƠNG TRÌNH HOÁ HỌC
1. Tính theo công thức hoá học
(1) Tính thành phần phần trăm về khối lượng hoặc khối lượng của mỗi nguyên tố trong hợp chất
a) Tính thành phần phần trăm về khối lượng của mỗi nguyên tố trong hợp chất
Giả sử có công thức hoá học đã biết AxBy ta tính được %A; %B:
%A = 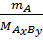 x 100% = x 100% = 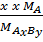 x 100% x 100% |
%B = 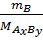 x 100% = x 100% = 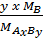 x 100% x 100% |
Trong đó:
- mA, mB là khối lượng của nguyên tố A và nguyên tố B,
- MA, MB và 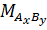 lần lượt là khối lượng mol của A, B và AxBy.
Nếu là hợp chất có nhiều nguyên tố, cách tính tương tự như trên.
b) Tính khối lượng của mỗi nguyên tố có trong một lượng chất đã cho:
Tính khối lượng của nguyên tố A trong hợp chất
lần lượt là khối lượng mol của A, B và AxBy.
Nếu là hợp chất có nhiều nguyên tố, cách tính tương tự như trên.
b) Tính khối lượng của mỗi nguyên tố có trong một lượng chất đã cho:
Tính khối lượng của nguyên tố A trong hợp chất 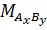 .
Trong
.
Trong 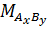 gam thì có mA gam hay x.MA gam nguyên tố A.
Vậy trong a gam AxBy thì có b gam nguyên tố A.
gam thì có mA gam hay x.MA gam nguyên tố A.
Vậy trong a gam AxBy thì có b gam nguyên tố A.
b = 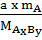 = = 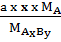 |
(2) Xác định công thức hoá học của hợp chất dựa vào thành phần về khối lượng của các nguyên tố trong hợp chất
a) Khi biết tỉ lệ về khối lượng của các nguyên tố trong hợp chất
Ví dụ 1: Tìm công thức hoá học (CTHH) của hợp chất khi phân tích được kết quả sau: Hiđro chiếm 1 phần về khối lượng, oxi chiếm 8 phần về khối lượng.
HƯỚNG DẪN GIẢI:
Cách 1: Giả sử công thức phân tử của hợp chất là HxOy.
Ta có tỉ lệ: 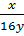 =
=  →
→  =
=  =
=  → CTHH của hợp chất là H2O
Cách 2: Giả sử khối lượng chất đem phân tích là a gam
mH chiếm:
→ CTHH của hợp chất là H2O
Cách 2: Giả sử khối lượng chất đem phân tích là a gam
mH chiếm:  → nH =
→ nH = 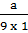 mO chiếm:
mO chiếm: 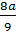 → nO =
→ nO = 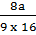 =
= 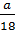
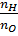 =
=  → CTHH là H2O
(Kí hiệu: m là khối lượng; n là số nguyên tử)
Vd 2: Tìm công thức hoá học của một oxit của sắt biết phân tử khối là 160, tỉ số khối lượng:
→ CTHH là H2O
(Kí hiệu: m là khối lượng; n là số nguyên tử)
Vd 2: Tìm công thức hoá học của một oxit của sắt biết phân tử khối là 160, tỉ số khối lượng: 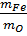 =
=  HƯỚNG DẪN GIẢI:
Cách 1:
nFe kết hơp với O =
HƯỚNG DẪN GIẢI:
Cách 1:
nFe kết hơp với O = 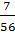 = 0,125 mol
nO kết hợp với Fe =
= 0,125 mol
nO kết hợp với Fe = 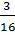 = 0,1875 mol
Như vậy: 0,125 mol nguyên tử Fe kết hợp với 0,1875 mol nguyên tử O. Suy ra 2 nguyên tử Fe kết hợp với 3 nguyên tử O.
Công thức hoá học đơn giản của oxit sắt là Fe2O3. Phân tử khối của Fe2O3 bằng 160.
Cách 2: Giả sử công thức hoá học của oxit là FexOy. Lập tỉ lệ khối lượng:
= 0,1875 mol
Như vậy: 0,125 mol nguyên tử Fe kết hợp với 0,1875 mol nguyên tử O. Suy ra 2 nguyên tử Fe kết hợp với 3 nguyên tử O.
Công thức hoá học đơn giản của oxit sắt là Fe2O3. Phân tử khối của Fe2O3 bằng 160.
Cách 2: Giả sử công thức hoá học của oxit là FexOy. Lập tỉ lệ khối lượng:
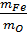 =
= 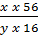 =
=  → y = 1,5x
x.56 + 1,5x.16 = 160 → x = 2; y = 3. Công thức hoá học: Fe2O3.
Nếu đề bài không cho biết phân tử khối ta dựa vào tỉ lệ
→ y = 1,5x
x.56 + 1,5x.16 = 160 → x = 2; y = 3. Công thức hoá học: Fe2O3.
Nếu đề bài không cho biết phân tử khối ta dựa vào tỉ lệ
 =
= 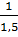 =
=  → x = 2; y = 3
b) Khi biết thành phần phần trăm về khối lượng các nguyên tố trong hợp chất
Trường hợp 1: Khi biết thành phần phần trăm về khối lượng của các nguyên tố và phân tử khối.
Giả sử công thức của hợp chất là AxBy, biết %A và %B. Cần tìm x và y.
Ví dụ 1: Xác định công thức oxit của lưu huỳnh biết phân tử khối của oxit là 80 và thành phần phần trăm về khối lượng của nguyên tố lưư huỳnh là 40%.
Cách 1: Lập tỉ số về khối lượng để tính các chỉ số x và y.
Giả sử công thức hoá học (CTHH) của oxit có dạng SxOy
→ x = 2; y = 3
b) Khi biết thành phần phần trăm về khối lượng các nguyên tố trong hợp chất
Trường hợp 1: Khi biết thành phần phần trăm về khối lượng của các nguyên tố và phân tử khối.
Giả sử công thức của hợp chất là AxBy, biết %A và %B. Cần tìm x và y.
Ví dụ 1: Xác định công thức oxit của lưu huỳnh biết phân tử khối của oxit là 80 và thành phần phần trăm về khối lượng của nguyên tố lưư huỳnh là 40%.
Cách 1: Lập tỉ số về khối lượng để tính các chỉ số x và y.
Giả sử công thức hoá học (CTHH) của oxit có dạng SxOy
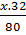 =
= 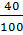 → x = 1;
→ x = 1; 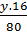 =
= 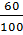 → y = 3 .
→ y = 3 . 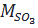 = 80
Công thức hoá học của oxit là SO3.
Cách 2: Vì khối lượng mỗi nguyên tố trong phân tử tỉ lệ với thành phần phần trăm nên ta có:
= 80
Công thức hoá học của oxit là SO3.
Cách 2: Vì khối lượng mỗi nguyên tố trong phân tử tỉ lệ với thành phần phần trăm nên ta có:
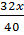 =
= 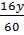 =
= 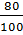 Giải ra ta có: x = 1; y = 3. Công thức hoá học của oxit là SO3.
Gặp bài toán tìm CTHH của hợp chất ta nên giải theo cách này.
Cách 3: Tìm số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
Trong 1 mol hợp chất có:
mS =
Giải ra ta có: x = 1; y = 3. Công thức hoá học của oxit là SO3.
Gặp bài toán tìm CTHH của hợp chất ta nên giải theo cách này.
Cách 3: Tìm số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
Trong 1 mol hợp chất có:
mS = 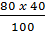 = 32g → nS =
= 32g → nS = 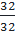 = 1
mO =
= 1
mO = 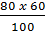 = 48g → nO =
= 48g → nO = 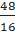 = 3
Suy ra 1 phân tử hợp chất có 1 nguyên tử S kết hợp với 3 nguyên tử O. CTHH: SO3
Ví dụ 2: Tìm công thức của hợp chất CxHyOzNt khi biết %C, %H, %O, %N và M.
Vì khối lượng mỗi nguyên tố trong phân tử tỉ lệ với thành phần phần trăm nên ta có:
= 3
Suy ra 1 phân tử hợp chất có 1 nguyên tử S kết hợp với 3 nguyên tử O. CTHH: SO3
Ví dụ 2: Tìm công thức của hợp chất CxHyOzNt khi biết %C, %H, %O, %N và M.
Vì khối lượng mỗi nguyên tố trong phân tử tỉ lệ với thành phần phần trăm nên ta có:
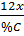 =
= 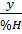 =
= 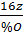 =
= 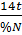 =
= 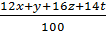 =
= 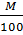 Từ đó ta có:
x =
Từ đó ta có:
x = 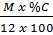 ; y =
; y = 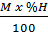 ; z =
; z = 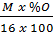 ; t =
; t = 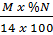 Trường hợp 2: Khi biết thành phần phần trăm về khối lượng các nguyên tố mà đề bài không cho biết phân tử khối (hoặc khối lượng mol).
Thí dụ: Hợp chất A chứa 3 nguyên tố Ca, C, O với tỉ lệ canxi chiếm 40%; C: 12%; O: 48% về khối lượng. Tìm công thức phân tử của A.
HƯỚNG DẪN GIẢI:
Giả sử lượng chất đem phân tích là a gam
mCa: =
Trường hợp 2: Khi biết thành phần phần trăm về khối lượng các nguyên tố mà đề bài không cho biết phân tử khối (hoặc khối lượng mol).
Thí dụ: Hợp chất A chứa 3 nguyên tố Ca, C, O với tỉ lệ canxi chiếm 40%; C: 12%; O: 48% về khối lượng. Tìm công thức phân tử của A.
HƯỚNG DẪN GIẢI:
Giả sử lượng chất đem phân tích là a gam
mCa: = 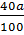 ⇒ nCa =
⇒ nCa = 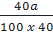 =
= 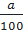 mC: =
mC: = 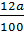 ⇒ nC =
⇒ nC = 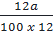 =
= 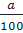 mO: =
mO: = 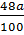 ⇒ nO =
⇒ nO = 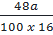 =
= 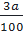 nCa : nC : nO =
nCa : nC : nO = 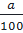 :
: 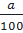 :
: 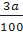 = 1 : 1: 3 ⇒ CTPT của A là CaCO3.
2. Những điểm cần lưu ý khi giải bài tập tính theo phương trình hoá học (PTHH)
- Sử dụng thành thạo công thức liên hệ giữa số mol, khối lượng mol, thể tích và thể tích 1 mol ở đktc
m = n.M; n =
= 1 : 1: 3 ⇒ CTPT của A là CaCO3.
2. Những điểm cần lưu ý khi giải bài tập tính theo phương trình hoá học (PTHH)
- Sử dụng thành thạo công thức liên hệ giữa số mol, khối lượng mol, thể tích và thể tích 1 mol ở đktc
m = n.M; n = 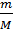 ; n =
; n = 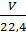 .
Trong đó: m là khối lượng (tính bằng gam) của một lượng nguyên tố hay một lượng chất nào đó; n là số mol; M là khối lượng mol (nguyên tử, phân tử...) 22,4 lít là thể tích mol khí ở đktc, V là thể tích khí ở đktc.
- Lập phương trình hoá học.
+ Viết đúng CTHH của các chất tham gia và tạo thành.
+ Chọn hệ số phân tử sao cho số nguyên tử của mỗi nguyên tố ở hai vế đều bằng nhau.
- Từ PTHH nhất thiết phải rút ra tỉ lệ số mol của chất cho biết và cần tìm.
(1) Trong những bài tính theo công thức và phương trình hoá học, khi chỉ biết lượng của một trong các chất tham gia hoặc tạo thành trong phản ứng là có thể tính được lượng của chất còn lại.
Lượng các chất có thể tính theo mol, theo khối lượng là gam, kilogam, tấn hoặc theo thể tích là mililit hoặc lít hoặc m3.
Lưụ ý: Tất cả các bài toán này đều tính theo cách lập quy tắc tam suất tỉ lệ thuận.
a) Bài toán tính theo số mol
Cho 32,5g Zn tác dụng vừa đủ với dung dịch HCl, tính thể tích khí hiđro sinh ra (đktc).
HƯỚNG DẪN GIẢI:
nZ =
.
Trong đó: m là khối lượng (tính bằng gam) của một lượng nguyên tố hay một lượng chất nào đó; n là số mol; M là khối lượng mol (nguyên tử, phân tử...) 22,4 lít là thể tích mol khí ở đktc, V là thể tích khí ở đktc.
- Lập phương trình hoá học.
+ Viết đúng CTHH của các chất tham gia và tạo thành.
+ Chọn hệ số phân tử sao cho số nguyên tử của mỗi nguyên tố ở hai vế đều bằng nhau.
- Từ PTHH nhất thiết phải rút ra tỉ lệ số mol của chất cho biết và cần tìm.
(1) Trong những bài tính theo công thức và phương trình hoá học, khi chỉ biết lượng của một trong các chất tham gia hoặc tạo thành trong phản ứng là có thể tính được lượng của chất còn lại.
Lượng các chất có thể tính theo mol, theo khối lượng là gam, kilogam, tấn hoặc theo thể tích là mililit hoặc lít hoặc m3.
Lưụ ý: Tất cả các bài toán này đều tính theo cách lập quy tắc tam suất tỉ lệ thuận.
a) Bài toán tính theo số mol
Cho 32,5g Zn tác dụng vừa đủ với dung dịch HCl, tính thể tích khí hiđro sinh ra (đktc).
HƯỚNG DẪN GIẢI:
nZ = 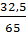 = 0,5 mol
Phương trình (pt) phản ứng:
Zn + 2HCl → ZnCl2 + H2
Theo pt: 1 mol 2 mol 1 mol
Theo đầu bài: 0,5 mol 0,5 mol
= 0,5 mol
Phương trình (pt) phản ứng:
Zn + 2HCl → ZnCl2 + H2
Theo pt: 1 mol 2 mol 1 mol
Theo đầu bài: 0,5 mol 0,5 mol
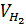 = 0,5 x 22,4 = 11,2 lít.
Chú ý:
- Nếu đầu bài yêu cầu tính lượng chất ra gam hoặc thể tích ra ml, lít thì các em cứ tính theo mol, sau đó đổi kết quả mol ra khối lượng hoặc thể tích.
- Nếu đầu bài cho dữ kiện lượng chất theo khối lượng hoặc theo thể tích mà hỏi kết quả là mol thì nên đổi khối lượng hoặc thể tích ra mol rồi tính.
b) Bài toán tính theo khối lượng là kg, tấn và thể tích là m3...
Với loại bài toán này không nên tính toán theo số mol như dạng
a) ở trên, mà tính theo khối lượng hoặc thể tích tương ứng với yêu cầu đề bài.
Ví dụ 1: Để khử độ chua của đất bằng CaO (vôi sống), người ta nung 10 tấn đá vôi trong lò vôi. Tính khối lượng CaO tạo thành. Coi hiệu suất phản ứng là 100%.
HƯỚNG DẪN GIẢI:
CaCO3
= 0,5 x 22,4 = 11,2 lít.
Chú ý:
- Nếu đầu bài yêu cầu tính lượng chất ra gam hoặc thể tích ra ml, lít thì các em cứ tính theo mol, sau đó đổi kết quả mol ra khối lượng hoặc thể tích.
- Nếu đầu bài cho dữ kiện lượng chất theo khối lượng hoặc theo thể tích mà hỏi kết quả là mol thì nên đổi khối lượng hoặc thể tích ra mol rồi tính.
b) Bài toán tính theo khối lượng là kg, tấn và thể tích là m3...
Với loại bài toán này không nên tính toán theo số mol như dạng
a) ở trên, mà tính theo khối lượng hoặc thể tích tương ứng với yêu cầu đề bài.
Ví dụ 1: Để khử độ chua của đất bằng CaO (vôi sống), người ta nung 10 tấn đá vôi trong lò vôi. Tính khối lượng CaO tạo thành. Coi hiệu suất phản ứng là 100%.
HƯỚNG DẪN GIẢI:
CaCO3 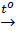 CaO + CO2
Theo pt: 100g 56g
Theo đầu bài: 10 tấn x tấn
x =
CaO + CO2
Theo pt: 100g 56g
Theo đầu bài: 10 tấn x tấn
x = 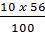 = 5,6 tấn
Ví dụ 2: Cho 10m3 khí oxi nguyên chất cháy hết với cacbon. Tính thể tích khí CO2 thu được. Các thể tích khí đều đo ở đktc.
HƯỚNG DẪN GIẢI:
Phương trình phản ứng:
C + O2 → CO2
Theo pt: 22,4 lít 22,4 lít
Theo đầu bài: 10 m3 y m3
(2) Trường hợp gặp bài toán cho biết lượng của cả hai chất tham gia và yêu cầu tính lượng chất tạo thành. Trong số hai chất tham gia phản ứng sẽ có một chất phản ứng hết, chất kia có thể phản ứng hết hoặc dư. Lượng chất tạo thành tính theo lượng chất nào phản ứng hết, do đó phải tìm xem trong hai chất cho biết chất nào phản ứng hết. Để xác định chất dư trong phản ứng ta nên lập tỉ số.
Ví dụ: Phương trình A + B → C + D
Cách xác định chất dư: Lập tỉ số
= 5,6 tấn
Ví dụ 2: Cho 10m3 khí oxi nguyên chất cháy hết với cacbon. Tính thể tích khí CO2 thu được. Các thể tích khí đều đo ở đktc.
HƯỚNG DẪN GIẢI:
Phương trình phản ứng:
C + O2 → CO2
Theo pt: 22,4 lít 22,4 lít
Theo đầu bài: 10 m3 y m3
(2) Trường hợp gặp bài toán cho biết lượng của cả hai chất tham gia và yêu cầu tính lượng chất tạo thành. Trong số hai chất tham gia phản ứng sẽ có một chất phản ứng hết, chất kia có thể phản ứng hết hoặc dư. Lượng chất tạo thành tính theo lượng chất nào phản ứng hết, do đó phải tìm xem trong hai chất cho biết chất nào phản ứng hết. Để xác định chất dư trong phản ứng ta nên lập tỉ số.
Ví dụ: Phương trình A + B → C + D
Cách xác định chất dư: Lập tỉ số
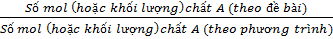
và
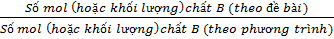 So sánh 2 tỉ số, tỉ số nào lớn hơn chất đó dư, chất còn lại phản ứng hết. Tính khối lượng chất (theo yêu cầu của đề bài) theo chất phản ứng hết.
Ví dụ: Cho 50g dung dịch NaOH tác dụng với 36,5g dung dịch HCl. Tính khối lượng muối tạo thành sau phản ứng.
HƯỚNG DẪN GIẢI:
nNaOH =
So sánh 2 tỉ số, tỉ số nào lớn hơn chất đó dư, chất còn lại phản ứng hết. Tính khối lượng chất (theo yêu cầu của đề bài) theo chất phản ứng hết.
Ví dụ: Cho 50g dung dịch NaOH tác dụng với 36,5g dung dịch HCl. Tính khối lượng muối tạo thành sau phản ứng.
HƯỚNG DẪN GIẢI:
nNaOH = 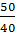 = 1,25 mol; nHCl =
= 1,25 mol; nHCl = 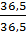 = 1 mol
Phương trình phản ứng:
NaOH + HCl → NaCl+ H2O
Theo pt: 1 mol 1 mol
Lập tỉ số:
= 1 mol
Phương trình phản ứng:
NaOH + HCl → NaCl+ H2O
Theo pt: 1 mol 1 mol
Lập tỉ số: 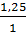 >
>  ⇒ nNaOH dư
Theo đầu bài: 1,25 mol 1 mol
Phản ứng: 1 mol 1 mol 1 mol
Theo phương trình trên và dữ kiện đề bài nNaOH dư, nên tính nNaCl theo nHCl (nghĩa là tính mNaCl theo mHCl).
mNaCl = 1 x 58,5 = 58,5g.
Chú ý: Nếu đầu bài cho dữ kiện chất tham gia hoặc chất tạo thành tính bằng mol mà kết quả lại yêu cầu tính bằng gam hoặc lít thì không thể đặt quy tắc tam suất như trên mà phải đổi moi ra khối lượng (gam) hoặc ra thể tích lít (hoặc dm3). Nếu không bài toán sẽ sai hoàn toàn, ví dụ như bài toán sau:
Cho 0,5 mol H2 tác dụng vừa đủ với O2 để tạo nước. Tính thể tích O2 cần (ở đktc).
2H2 + O2 → 2H2O
2 mol cần 1 mol
0, 5 mol x mol
x =
⇒ nNaOH dư
Theo đầu bài: 1,25 mol 1 mol
Phản ứng: 1 mol 1 mol 1 mol
Theo phương trình trên và dữ kiện đề bài nNaOH dư, nên tính nNaCl theo nHCl (nghĩa là tính mNaCl theo mHCl).
mNaCl = 1 x 58,5 = 58,5g.
Chú ý: Nếu đầu bài cho dữ kiện chất tham gia hoặc chất tạo thành tính bằng mol mà kết quả lại yêu cầu tính bằng gam hoặc lít thì không thể đặt quy tắc tam suất như trên mà phải đổi moi ra khối lượng (gam) hoặc ra thể tích lít (hoặc dm3). Nếu không bài toán sẽ sai hoàn toàn, ví dụ như bài toán sau:
Cho 0,5 mol H2 tác dụng vừa đủ với O2 để tạo nước. Tính thể tích O2 cần (ở đktc).
2H2 + O2 → 2H2O
2 mol cần 1 mol
0, 5 mol x mol
x = 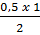 = 0,25 lít
Kết quả sai hoàn toàn. Vậy phải tính x ra mol sau đó nhân với 22,4 lit.
III. TÍNH HIỆU SUẤT PHẢN ỨNG
Thực tế do một số nguyên nhân chất tham gia phản ứng không tác dụng hết, nghĩa là hiệu suất dưới 100%. Người ta có thể tính hiệu suất phản ứng như sau:
a) Dựa vào một trong các chất tham gia phản ứng:
Công thức tính:
H% =
= 0,25 lít
Kết quả sai hoàn toàn. Vậy phải tính x ra mol sau đó nhân với 22,4 lit.
III. TÍNH HIỆU SUẤT PHẢN ỨNG
Thực tế do một số nguyên nhân chất tham gia phản ứng không tác dụng hết, nghĩa là hiệu suất dưới 100%. Người ta có thể tính hiệu suất phản ứng như sau:
a) Dựa vào một trong các chất tham gia phản ứng:
Công thức tính:
H% = 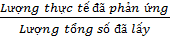 x 100%
Chú ý: Chỉ áp dụng công thức này đối với chất tham gia phản ứng lẽ ra phải hết mà không áp dụng với các chất đầu bài cho dư.
b) Dựa vào một trong các chất tạo thành:
Công thức tính:
H% =
x 100%
Chú ý: Chỉ áp dụng công thức này đối với chất tham gia phản ứng lẽ ra phải hết mà không áp dụng với các chất đầu bài cho dư.
b) Dựa vào một trong các chất tạo thành:
Công thức tính:
H% = 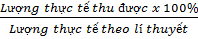
© Bản quyền thuộc về
Bài kiểm tra. Ghi rõ nguồn Bài kiểm tra.com khi sao chép nội dung này.