© 2020 Bài Kiểm Tra.com. All Rights Reserved.
Đề thi học kì 2 môn Toán 1 sách Chân trời năm 2024, có đáp án kèm theo.

Đề thi học kì 2 môn Tiếng Việt 3 sách Chân trời năm 2024, có đáp án kèm theo.

Đề thi học kì 2 môn Lịch sử và Địa lí 4 sách Chân trời. Đề thi gồm 2 phần trắc nghiệm và tự luận. Có đáp án và hướng dẫn chấm điểm

Mỗi lần được ra ngoài trải nghiệm các hoạt động thực tế cùng người thân, em luôn cảm thấy hào hứng, phấn khởi.

Đề thi học kì 2 môn Công Dân 7 sách Cánh diều, có đáp án kèm theo.

Đề thi học kì 2 môn Tin học 8 sách Chân trời năm 2024, có đáp án kèm theo.

Từ bao đời nay, thiên nhiên là nguồn sống vô tận của con người: cơm, gạo, thịt, cá, cây trái, nhà để ở, nước để uống, quần áo để mặc, khí trời để thở… đều do thiên nhiên cung cấp.

Trọn bộ giáo án cả năm Âm nhạc 1 sách: Chân trời sáng tạo. Gồm 8 chủ đề: Chủ đề 1 : Âm thanh ngày mới; Chủ đề 2 : Nhịp điệu tuổi thơ; Chủ đề 3 : Bài ca lao động; Chủ đề 4 : Tiếng ca muôn loài; Chủ đề...

Đề cương ôn tập kiểm tra học kì 2, môn: Tiếng Anh 11, đề cương gồm các phần: Phát âm, từ vựng, ngữ pháp, giới từ, câu hỏi, viết, đọc, nghe, nói,...

Giải Công dân 7 sách Chân trời sáng tạo, bài 11: Phòng, chống tệ nạn xã hội - Trang 56, 57, 58, 59, 60.

Giải Công nghệ 6 sách Kết nối tri thức: Ôn tập chương 4 - Trang 74.
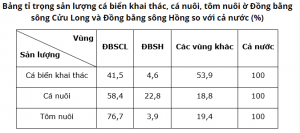
Đề cương ôn tập kiểm tra học kì 2, môn: Địa lí 9, đề gồm hai phần trắc nghiệm và tự luận. Có đáp án trắc nghiệm (phần in đậm) và hướng dẫn giải.

Đề kiểm tra học kì 2, môn: Hoá học 12, đề trắc nghiệm, có đáp án. Mời các anh/chị cùng luyện tập và thi tốt.

Đề thi học kì 2 môn Lịch sử & Địa lí lớp 5, có đáp án kèm theo.

Đề cương ôn tập cuối học kì 2, Sinh học 9, gồm hai phần Tự luận và Trắc nghiệm. Không đáp án. Mời các em cùng ôn tập để thi tốt học kì 2 nhé!

Giải Tin học 6 sách Kết nối, bài 17: Chương trình máy tính - Trang 71, 72, 73, 74.

Tuyển tập 10 đề thi cuối học kì 2 môn: Toán 5. Đề gồm 2 phần trắc nghiệm và tự luận, có đáp án và hướng dẫn chấm điểm. Các em tự luyện tập nhé!

Thi phẩm "Đồng dao mùa xuân" của nhà thơ Thanh Thảo đã để lại cho em nhiều suy nghĩ về hình ảnh người lính thời chiến và người lính trong thời bình bây giờ. Tuy có khác nhau về thời gian lịch sử nhưng...

Đề cương ôn tập kiểm tra học kì 2, môn: Vật lí 8, đề cương gồm hai phần lí thuyết và bài tập. Có đáp án và hướng dẫn giải.

Giáo án cả năm: Giáo dục quốc phòng - an ninh 12, trọn bộ cả năm. Mời các bạn cùng tham khảo.

Trọn bộ đáp án các môn thi tốt nghiệp TPHT năm 2023 của Bộ GD&ĐT, gồm các môn: Toán, Ngữ Văn, Tiếng Anh, Lịch sử, Địa lí, Giáo dục công dân, Sinh học, Vật lí, Hoá học

Bài dự thi viết thư Quốc tế UPU lần thứ 53, chủ đề: Viết thư cho các thế hệ tương lai về thế giới mà bạn hy vọng họ sẽ thừa hưởng

Giáo dục học mầm non là một chuyên ngành của giáo dục học có nhiệm vụ nghiên cứu, xây dựng lý luận và chỉ đạo việc tổ chức các hoạt động thực tiễn chăm sóc giáo dục trẻ mầm non từ 0 - 6 tuổi.

Giáo án lao động, lớp 8: nội dung lao động vệ sinh trường. Giáo dục HS có ý thức giữ gìn vệ sinh chung, ý thức xây dựng cảnh quan môi trường sạch đẹp.

Đề tài tiểu luận của học phần Triết học: “Nội dung và ý nghĩa của mối liên hệ giữa cái chung và cái riêng đối với nghề nghiệp bản thân”.

Đề cương ôn tập cuối học kì 2, Khoa học 5, gồm hai phần trắc nghiệm và tự luận, có đáp án và hướng dẫn giải. Chúc các em ôn tập tốt.

Hướng dẫn soạn giảng Đạo đức lớp 1 - Bài 8. Quan tâm chăm sóc cha mẹ, Chủ đề 3: Quan Tâm Chăm Sóc Người Thân Gia Đình, trong bộ sách: Đạo đức 1 - Kết nối tri thức với cuộc sống.

Đề thi học kì 2 môn Toán 2 sách Kết nối năm 2024, có đáp án kèm theo.